201、转甲状腺素蛋白淀粉样变性
罕见病诊疗指南(2025年版)
概述 转甲状腺素蛋白淀粉样变(transthyretin amyloidosis,ATTR)是由于不稳定的转甲状腺素蛋白(transthyretin,TTR)沉积所致的系统性疾病。TTR由肝脏合成,正常情况下为四聚体,病理状态下解离成单体后错误折叠为淀粉样物质,沉积于组织间质,导致ATTR。主要累及的器官为周围神经和心脏,表现为运动和感觉神经异常以及自主神经功能异常、左室肥厚和心力衰竭。
病因和流行病学
TTR的异常解聚是该病发生的核心机制。TTR主要由肝脏产生,以四聚体形式携带转运甲状腺素和视黄素,如果解离为单体并错误折叠产生不可溶性淀粉样物质,沉积于器官或组织的细胞间质中导致其功能异常。淀粉样物质沉积带来的物理破坏以及淀粉样蛋白的毒性是损伤脏器功能的主要机制。
根据有无基因突变分为遗传型或突变型ATTR(mutant, ATTRm)和野生型(wild type,ATTRwt)。ATTRm是由TTR基因突变所致,氨基酸序列发生改变的TTR蛋白稳定性降低,容易发生解离并错误折叠为淀粉样纤维。目前被认为是一种罕见病,估计在全球范围内有50000名患者。ATTRm为常染色体显性遗传,迄今发现已有140多个TTR 基因突变。其中以Val30Met突变最为常见,其次为Val122Ile。常见的表型是周围神经病变、心肌病或混合型。ATTRwt患者的TTR蛋白氨基酸排列无异常,蛋白发生解离的原因尚未阐明,但推测与异常的蛋白质动力学和衰老相关的翻译后修饰相关。ATTRwt主要影响老年人,通常是70~75岁以上的老年人,90%是男性。虽然不能准确估计ATTRwt的患病率,但在某些患者群体中似乎并不少见。一项85岁以上人群的尸检研究显示25%受检者的心脏中有TTR沉积。在60岁以上射血分数保留心力衰竭(heart failure with preserved ejection fraction, HFpEF)和左室肥厚(≥12mm)的患者中进行99mTc-DPD核素扫描检测,13.3%最终诊断为ATTRwt心脏淀粉样变(cardiac amyloidosis, CA)。在接受经导管主动脉瓣置换术的老年人中,由99mTc-DPD或者99mTc-PYP核素检测发现16%合并ATTRwt。ATTRwt几乎主要累及心脏,导致心室壁增厚、进行性心力衰竭和心律失常。ATTRm的预后根据突变类型、原纤维类型以及家族史而有显著差异。然而,主要预后决定因素为心脏受累,ATTRm-CA患者确诊后的中位生存期为2.5~3.5年,而仅表现为多发性神经病变的患者的中位生存期为8~10年。ATTRwt诊断后中位生存期4~5年。
临床表现
ATTR主要表现为周围神经病变(运动神经、感觉神经和自主神经)和/或心脏病变,其他不太常见的ATTRm临床表现包括眼部异常(包括导致视力逐渐丧失的玻璃体混浊和导致慢性开角型青光眼的小梁网阻塞)、中枢神经系统(脑膜受累)和肾脏受累(尿蛋白和肾功能异常)。ATTRwt心脏外受累主要表现为腕管综合征、椎管狭窄和肱二头肌肌腱断裂。
1.转甲状腺素蛋白淀粉样变性多发性神经病(transthyretin amyloid polyneuropathy,ATTR-PN) ATTR-PN的起病年龄跨度很大,我国人群的起病年龄在17~68岁,平均42岁。以起病年龄50岁为界,分为早发型和晚发型。
(1)感觉运动神经病:感觉障碍早于运动障碍。约80%的ATTR-PN患者出现慢性长度依赖性感觉运动神经病,多数患者的感觉和运动神经病为对称性。一般从四肢远端浅感觉减退、感觉异常或感觉过敏开始,下肢早于上肢,逐渐向近端发展。而后出现深感觉障碍,表现为感觉性共济失调。最后出现四肢远端为主的肌肉无力和萎缩,逐渐丧失行走能力。
(2)自主神经病:约90%的ATTR-PN患者出现自主神经病。早发型患者的自主神经受累更加突出。可以出现胃肠道系统、心血管系统、泌尿生殖系统及皮肤的自主神经功能障碍。患者可以出现腹泻、便秘、腹泻便秘交替、胃瘫及进食后呕吐,进一步导致脱水、营养不良、体重下降,严重时导致恶病质。还会出现直立不耐受及晕厥等直立性低血压症状,排尿障碍及性功能障碍,少汗、无汗等。
2.转甲状腺素蛋白心脏淀粉样变(transthyretin cardiac amyloidosis,ATTR-CA) 约50%~80%的ATTR患者出现心脏损害,是主要致死原因之一。主要表现为限制型心肌病和/或心力衰竭和心律失常。临床表现主要是活动后气短和右心力衰竭(颈静脉充盈、腹水和外周性水肿),超声心动图显示室壁增厚合并明显的舒张功能异常。射血分数通常大于50%,但是随着TTR的进一步沉积,射血分数可以降低。此外患者还可出现心律失常,包括房颤和传导阻滞。ATTR-CA的直立性低血压发生率约为11%,由于心排量减低和心律失常,还可引起晕厥和心源性猝死。心源性栓塞也可出现,甚至可以是首发表现。此外主动脉瓣狭窄也可以是ATTR的表现之一,特别是ATTRwt,合并率为6%~16%,老年低流速、低压力阶差的重度主动脉瓣狭窄,要考虑到ATTRwt的可能
3.其他表现
(1)眼部损害:约24%的ATTR-PN患者出现眼部损害。玻璃体混浊及小梁网阻塞导致的青光眼较为常见,引起视力下降,甚至失明。其他眼部异常包括神经营养性角膜炎、花边样瞳孔、缺血性视神经视网膜病变等。
(2)中枢神经系统损害:较为少见,一般在起病10年后出现,少数患者以此为首发表现。是由软脑膜淀粉样血管病引起的,可引起局灶性神经功能缺损、癫痫、脑出血、蛛网膜下腔出血、脑梗死、脑积水和痴呆等。
(3)其他:淀粉样物质易沉积于腰椎管及腕管软组织引起腰椎管狭窄和双侧腕管综合征。前者发生率约为14%,后者的发生率可以高达33%~60%。而且腕管综合征可以发生在心脏症状出现前10年左右。
辅助检查
1.一般检查 基于鉴别诊断,需要选择下列相关检查:血、尿、便常规、肝肾功能、尿蛋白定量、血糖、糖耐量试验、血维生素B12、血同型半胱氨酸、感染筛查、抗核抗体、抗可溶性抗原抗体谱、血尿免疫固定电泳、血游离轻链、脑脊液检查等。对于心脏受累需要检测利钠肽、肌钙蛋白,是评价CA严重程度的生物标记物,二者与其预后相关。
2.心电图 CA的典型心电图表现为QRS波低电压以及假性梗死征象。没有低电压并不能排除ATTR-CA。传导阻滞和房颤是ATTR-CA患者常见的心律失常。
3.超声心动图 提示CA可能的征象包括:双房增大、心室壁增厚(左右室壁均可)而心室腔无明显扩大、心肌内颗粒样强回声、房室瓣增厚、房间隔增厚、少量心包积液以及限制性舒张功能异常等。应变显像(表现为纵向应变峰值绝对值减低)可以更早地发现收缩功能异常,尤其是出现特征性的“心尖保留”模式,即左室基底和中段的纵向应变(longitudinal strain, LS)降低而心尖部正常。超声心动图能够提示CA,但不能准确区分AL和ATTR。
4.电生理检查 ATTR-PN患者早期出现小纤维神经病,可进行交感皮肤反应、定量感觉测定。交感皮肤反应可见潜伏期延长和波幅下降。定量感觉测定可见温度觉和震动觉阈值升高。随着疾病的进展,常规神经传导检查可以发现以轴索损害为主的感觉运动神经病,主要为感觉神经动作电位波幅下降。运动神经传导异常,表现为复合肌肉动作电位波幅下降,少数患者伴随远端潜伏期延长、神经传导速度减慢及异常波形离散。针极肌电图可以发现所检肌肉神经源性损害,以四肢远端肌肉受累明显。
5.CMR 不仅可以评价心脏的结构和功能,还能够显示心肌的组织特征。CMR显示ATTR-CA患者存在左室肥厚或者常合并右心室肥厚。CA钆延迟显像的典型表现是广泛的心内膜下LGE,不符合冠状动脉供血的区域分布。也可以表现为弥漫性透壁或者心肌内片状LGE。对于合并肾功能异常患者,可选用无对比剂T1 Mapping技术(native T1 mapping)测量心肌固有信号,ATTR患者的native T1值显著高于肥厚型心肌病。注射钆增强剂后,可以计算得出细胞外体积分数(extracellular volume fraction,ECV)。同样,ATTR患者的ECV也显著高于肥厚型心肌病。联合native T1和ECV可以更好地诊断ATTR,ECV还能独立预测ATTR患者的死亡风险。但是同样CMR不能准确区分AL和ATTR。
6.放射性核素骨闪烁扫描术 最初用于骨显像的锝[99Tcm]磷酸盐衍生物被发现可以与心脏组织中的TTR紧密结合,可能与TTR纤维中较高的钙成分相关。研究显示在临床疑诊CA患者中进行99Tcm焦磷酸盐(technetium pyrophosphate,99Tcm-PYP)显像,如果心肌摄取为2级或3级同时血清/尿液中单克隆免疫球蛋白阴性,诊断ATTR-CA的特异度和阳性预测值均为100%,并可在超声心动图或CMR出现异常之前就能识别出心肌病变。2级是指心肌摄取等于肋骨摄取,3级是指摄取大于肋骨摄取,伴有肋骨摄取明显减低/肋骨无摄取。
7.活检 心内膜心肌活检是诊断CA的金标准,刚果红染色是目前最常用的检测淀粉样变的病理学方法。淀粉样蛋白在苏木素-伊红染色光镜下表现为心肌间质内的均匀粉染、无细胞结构的嗜酸性物质。由于其ß褶片状结构,会与线性染料刚果红结合,并在偏振光下呈现苹果绿的双折射。淀粉样纤维在电子显微镜下为随机排列的无分支纤维,直径约为7.5~10 nm,可以作为光镜的补充。心脏外组织活检的阳性率取决于淀粉样变的类型和所检查的组织,例如脂肪活检的阳性率ATTRm型为67%,而ATTRwt型仅为14%。因此,脂肪活检阴性结果不足以排除ATTR-CA诊断,应考虑进行心内膜心肌活检。不同组织活检阳性率不一,唾液腺(91%)、周围神经(80%)、心脏(约100%)、肾脏(92%~100%)、皮肤(70%)、腹部皮下脂肪(14%~83%),可根据病变受累的脏器严重程度及操作难易程度、可及性等选择不同的脏器进行活检,必要时可多次或联合多部位活检以提高阳性率。
刚果红染色阳性显示为淀粉样变,随后应该确定淀粉样纤维的前体蛋白类型,可以通过免疫组织化学或激光显微切割和/或质谱完成。免疫组织化学是最广泛使用的蛋白分型方法,但是灵敏度较低,而且容易出现ATTR假阳性。激光显微切割和/或质谱技术可以对淀粉样变进行准确的诊断和分型,是淀粉样纤维的前体蛋白分型新的金标准。
8.基因检测 建议所有确诊为ATTR的患者均进行基因检测,因为不完全外显和晚发导致家族史缺失的情况下,仅凭临床检查和组织学技术无法区分ATTRm和ATTRwt。致病突变基因的发现对ATTRm预后、治疗选择、家族筛查和遗传咨询都有重要作用。
诊断
1.ATTR-PN诊断
(1)诊断标准包括以下3条:①慢性感觉性神经病和/或慢性自主神经病,伴或不伴运动性神经病,可同时合并心脏、眼部、肾脏或中枢神经系统损害,有或无家族史。②病理检查发现组织内淀粉样物质沉积,证实为转甲状腺素蛋白沉积,或基因检测发现TTR基因致病变异。③排除其他疾病,需要鉴别的疾病包括但不限于成年发病的慢性炎性脱髓鞘性多发性神经根神经病、慢性特发性轴索性神经病、糖尿病性神经病、慢性酒精中毒性神经病、副肿瘤性神经病、轻链型淀粉样变性周围神经病。ATTR-PN最常被误诊为慢性炎性脱髓鞘性多发性神经根神经病或慢性特发性轴索性神经病。这些疾病通过一般检查和正确解读电生理检查结果可以初步鉴别,进一步采取组织病理学检查和基因分析是诊断ATTR PN的关键
(2)临床严重程度分级(表80-1)
表80-1 转甲状腺素蛋白淀粉样变性多发性神经病临床严重程度分期和分级
分期 | 症状 | 改良多发性神经病残障评分 |
0期 | 无症状 |
|
1期 | 可独立行走,症状局限于下肢 | 1级,四肢感觉障碍,行走正常 2级,行走出现障碍,但是不需要帮助 |
2期 | 行走需要帮助 | 3a级,行走需1根拐杖3b级,行走需2根拐杖 |
3期 | 坐轮椅或卧床 | 4级,坐轮椅或卧床 |
2.ATTR-CA诊断
(1)ATTR-CA的“警示征”:对于有左室肥厚(室壁厚度≥12mm)同时具有1条以上特征的患者应该考虑到是否有CA特别是ATTR-CA可能。
1)心力衰竭(射血分数≥40%),左室无扩大;
2)超声心动图显示左室肥厚而心电图无QRS高电压表现;
3)肌钙蛋白持续低水平升高;
4)老年人低压差、低流速主动脉瓣狭窄,伴右室肥厚;
5)因低血压(特别是体位性低血)不耐受血管紧张素系统抑制剂和/或β受体阻滞剂;
6)多发周围神经病变,特别是伴有自主神经功能异常(不明原因腹泻与便秘、体位性低血压,尿潴留、尿失禁等);
7)家族性周围神经病变;
8)老年人双侧腕管综合征和/或腰椎管狭窄;
9)反复双眼白内障。
(2)诊断流程
对于出现以上“警示征”的高危人群,可考虑进入以下ATTR-CA确诊流程:①完善心电图、超声心动图和CMR检查。如果心电图、超声心动图和CMR高度提示CA可能,则进入以下步骤。②单克隆免疫球蛋白检测:如果单克隆免疫球蛋白检测无异常,可进行99mTc-PYP进行确诊。不具备核素扫描检查或者99mTc-PYP结果无法明确时,建议行侵入性心内膜心肌组织活检进行确诊。如血清FLC比值异常、血清/尿IFE阳性,应请血液科会诊。③患者确诊ATTR-CA后经还需基因检测有无TTR基因突变。
鉴别诊断
CA可能会被误诊为其他原因导致的心肌肥厚,例如肥厚型心肌病和高血压导致的左室肥厚以及心力衰竭,特别是射血分数保留的心力衰竭。CA患者可以出现血清肌钙蛋白升高,要注意与急性冠脉综合征进行鉴别。诊断CA时需要区分是AL型还是ATTR型。诊断AL-CA的必要条件是体内检测到单克隆免疫球蛋白,鉴定的方法包括血清游离轻链(free light chain, FLC)和血清/尿免疫固定电泳( immunofixation electrophoresis, IFE)。单独每项检查对单克隆免疫球蛋白的检出率为69%~91%,血清FLC联合血和尿IFE的检出率可以达到98%~99%。由于灵敏度低,不推荐血清蛋白电泳用于筛查单克隆免疫球蛋白。
临床严重程度分级(表80-2)。
表80-2 转甲状腺素蛋白心脏淀粉样变临床严重程度分期和分级
| 梅奥分期 | 英国国家淀粉样变中心分期 |
危险因素 | cTnT≥0.05ng/ml NT-proBNP≥3000pg/ml | NT-proBNP>3000pg/ml eGFR<45ml/min |
1级 | 无危险因素 | 无危险因素 |
2级 | 1个危险因素 | 1个危险因素 |
3级 | 2个危险因素 | 2个危险因素 |
治疗
1.器官移植
(1)原位肝移植(orthotopic liver transplantation,OLT):OLT是治疗ATTR最早且有效的方法,通过移植正常肝脏组织可以终止突变型TTR的生成。已经证实OLT能够延长ATTRm患者生存期,V30M患者10年生存率为73%,非V30M患者10年生存率为52%。然而OLT也具有局限性,如移植后疾病仍可能进展(特别是非V30M突变患者的心脏淀粉样变)、需要等待供体、长期免疫抑制治疗等均对患者造成负担。
(2)多器官移植:少数ATTR患者在OLT同时进行了心脏或肾脏移植。肝脏和心脏/肾脏移植联合治疗的患者比仅移植肝脏的患者生存期可长5年。尤其对于并发心脏受累者,可以考虑肝脏-心脏联合移植。但多器官移植后仍然可能会发生缓慢的神经病变进展。并且由于需要等待更多的供体及免疫抑制治疗,负担可能更重。
2.药物治疗
(1)TTR稳定剂
1)氯苯唑酸:是一种小分子口服药物,与TTR结合后,可减少四聚体解离,从而抑制TTR淀粉样蛋白原纤维形成。Ⅲ期随机对照研究(randomized control trail,RCT)显示在30个月的治疗期间,氯苯唑酸显著降低了ATTR-CA患者的全因死亡和心血管相关住院率。之后包括我国在内多个国家批准氯苯唑酸(61mg q.d.)用于治疗ATTR-CA合并心衰。早期V30M患者使用氯苯唑酸(20mg q.d.)可以保留患者的生活质量、减慢下肢神经功能障碍的进展速度;而晚期V30M患者无明显获益;非V30M患者的神经功能障碍仍持续进展,但生活质量、营养状况及心功能均维持稳定。鉴于以上临床试验结果,我国和欧洲、日本等国家批准氯苯唑酸(20mg q.d.)用于治疗ATTR-PN。
2)AG10(acoramids):也是一种口服的小分子药物,能够与TTR四聚体以强的氢键结合,有效稳定TTR四聚体,减少淀粉原纤维的形成。Ⅱ期RCT证实AG10可有效稳定ATTR-CA患者的N末端B型利钠肽原和心肌肌钙蛋白I(cTnI)。由于该研究主要是观察AG10的安全性和药代动力学,且研究仅28 d,因此未评价心脏影像学指标和预后。 Ⅲ期RCT研究显示AG10每日2次,每次800mg能够降低ATTR-CA患者的复合临床终点(死亡、心血管相关的住院、NT-probnp较基线变化和6分钟步行距离较基线变化)。美国FDA批准该药用于治疗ATTR-CA。
3)二氟尼柳:非甾体消炎止痛药,能一定程度上延缓神经功能障碍的恶化程度,稳定心脏功能,目前并未获批治疗ATTR。临床中1期和2期PN患者如果无法获得其他治疗药物,可以应用该药物。常规剂量为每日2次,每次250mg口服。长期应用有消化道出血、肾功能衰竭、心力衰竭副作用,需要注意监测。GFR<45ml/min、严重心功能不全禁用。
(2)基因沉默药物
1)patisiran:是一种小干扰RNA,以序列特异方式与靶信使RNA(mRNA)结合,通过酶降解起到敲除的作用,从而阻断TTR蛋白的生成。RCT显示patisiran治疗18个月 能够减少ATTRm-PN患者周围神经中淀粉样沉积物的积累,改善患者神经病变(包括自主神经)的评分和步态速度。欧盟和美国FDA已经批准patisiran治疗轻中度ATTRm-PN。Patisiran在ATTR-CA患者中进行的III期临床研究显示,治疗12个月,相较于安慰剂可以使6分钟步行距离的下降更少,改善生活质量评分。该药需要每3周静脉输注一次,主要不良反应与输液相关,包括背痛、恶心、腹痛、呼吸困难、潮红和头痛、上呼吸道感染等以及维生素A缺乏。
2)vutrisiran:为第二代小干扰RNA,每3个月皮下注射一次。RCT证实vutrisiran治疗9个月可以改善ATTRm-PN患者的神经病变。美国和欧盟批准vutrisiran用于治疗ATTRm-PN。在ATTR-CA患者中的III期临床研究显示,与安慰剂相比,vutrisiran可以降低全因死亡和心血管事件风险,改善心功能和生活质量。该药物最常见的不良反应是关节僵硬以及手臂和腿部疼痛。
3)inotersen:是一种反义寡核苷酸药物,是含20个左右核苷酸的单链寡聚物,以序列特异方式与编码TTR蛋白的mRNA相结合,导致mRNA降解,抑制TTR蛋白生成,从而降低TTR蛋白水平。在ATTRm-PN患者中进行的Ⅲ期RCT表明,无论患者属于何种突变类型或处于何种神经病变阶段,inotersen治疗15个月可使TTR蛋白水平显著降低,同时改善ATTRm患者的神经系统评分和生活质量。Inotersen获得美国和欧盟批准用于治疗ATTRm-PN,每周皮下注射一次,其主要不良反应是肾小球肾炎和血小板减少,尤其后者需增强监测。目前尚无针对此研究心肌病亚组的分析结果。Inotersen治疗ATTR-CA的Ⅱ期RCT正在进行。
4)eplontersen:是一种配体偶联反义寡核苷酸药物,一月一次皮下注射。Ⅲ期RCT也证实其治疗66周可以改善ATTRm-PN患者的神经系统评分和生活质量,并显示出良好的安全性。美国和欧盟批准其用于治疗ATTRm-PN。eplontersen目前正在ATTR-CA患者中进行Ⅲ期RCT。
3.基因编辑 NTLA-2001是一种基于CRISPR-Cas9的体内基因编辑疗法,由一个具有肝脏取向性的专有脂质纳米粒(LNP)输送系统组成,携带一个靶向人类TTR基因的单链RNA(sgRNA)和一个人类密码子优化的化脓性链球菌Cas9蛋白mRNA序列。通过静脉输注给药,到达肝脏后编辑肝细胞中的TTR基因,使得单次给药后TTR蛋白产生有所减少。Ⅰ期临床研究纳入6名ATTRm患者,3名患者接受0.1mg/kg剂量,3例患者接受0.3mg/kg剂量,接受治疗28天后,两种不同剂量的患者血清中TTR蛋白水平分别平均下降52%和87%,下降幅度在12个月随访时间里持续稳定。治疗未观察到严重不良反应。这是世界首例在人体内进行的CRISPR基因编辑临床试验。NTLA-2001的III期临床研究目前正在进行中。
4.清除淀粉样纤维
(1)多西环素和牛磺熊去氧胆酸(TUDCA):已被证实能破坏ATTR纤维,从而促进组织巨噬细胞对淀粉样沉积物的再吸收。小型多西环素联合熊去氧胆酸治疗ATTR患者的临床研究,但由于治疗无效和不良反应导致脱落率较高,其疗效未得到证实。目前在ATTR-CA患者中进行Ⅲ期RCT研究。
(2)PRX004:是一种人源化单克隆抗体,只与TTR蛋白单体中暴露的表位结合,通过抗体介导的吞噬作用,促进不溶性TTR淀粉样蛋白原纤维的清除并抑制淀粉样蛋白的形成。Ⅰ期研究初步显示PRX004改善了ATTR患者的神经病变和心脏收缩功能。该药物目前正在进行II期临床试验。
(3)NI006:也是人源化单克隆抗体,特异性靶向错误折叠的转甲状腺素蛋白,介导巨噬细胞对TTR纤维进行吞噬,清除组织中TTR沉积物。在ATTR-CA患者的1期RCT显示,NI006的安全性良好,未观察到明显的剂量相关毒性或与药物相关的严重不良反应。骨闪烁扫描术或心脏磁共振成像检测结果显示,在至少10 mg/kg的剂量下,患者心脏淀粉样蛋白负荷在12个月内显著减少。此外,N末端B型钠尿肽原和肌钙蛋白T的水平也有所降低。目前该药物正在进行全球多中心的III期RCT研究。
诊疗流程(图80-1,图80-2)
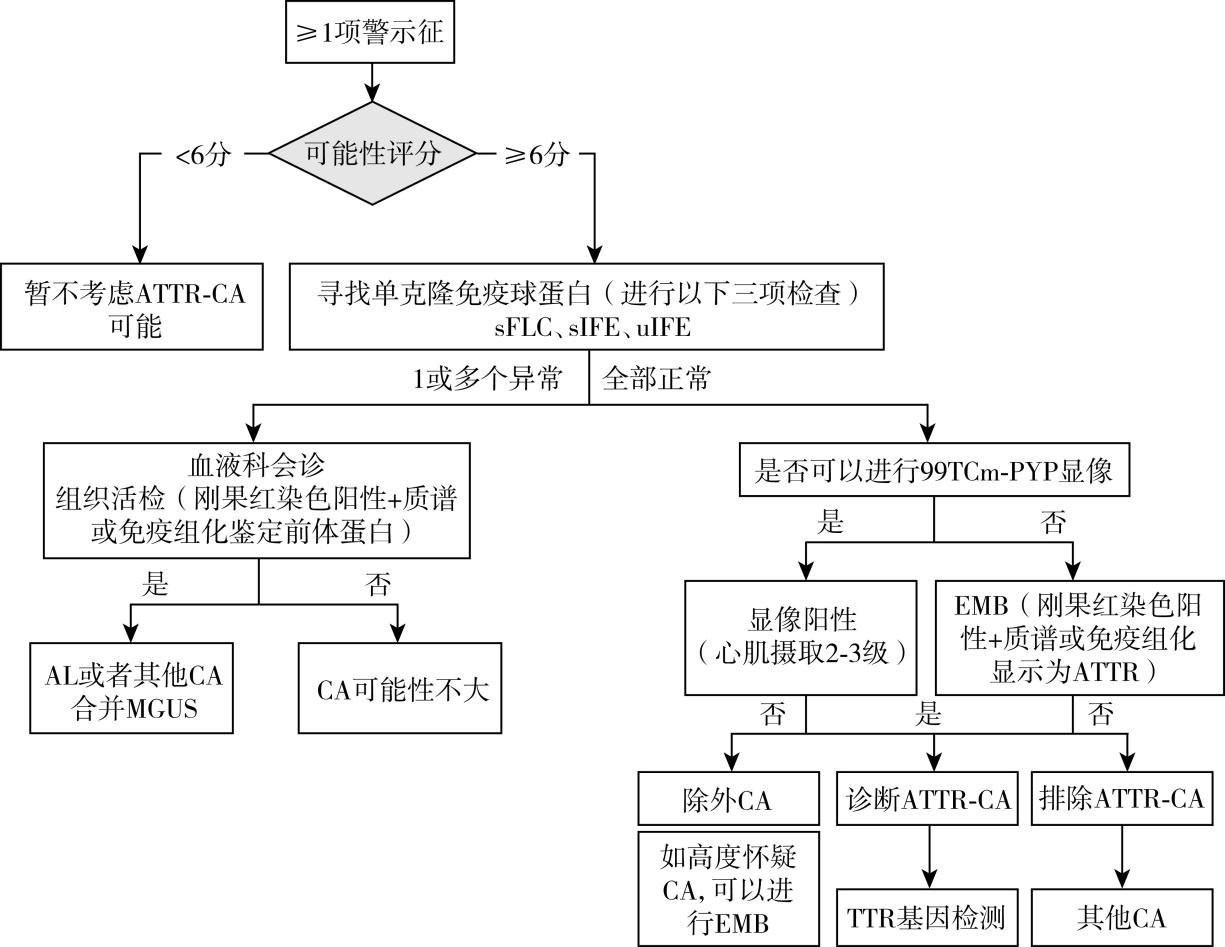
图80-1 ATTR-PN诊断流程
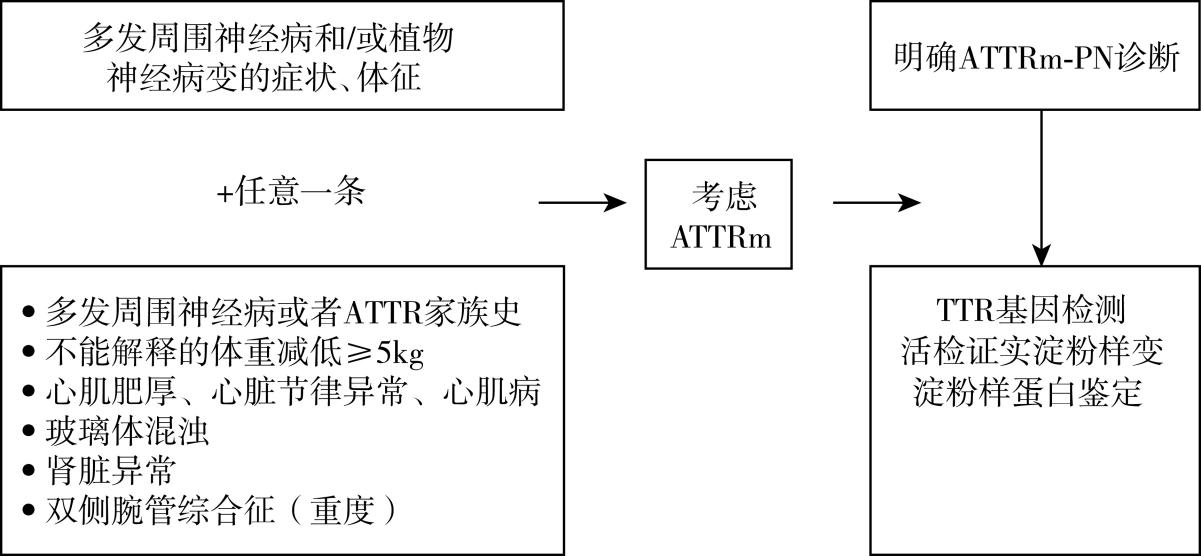
图80-2 转甲状腺素蛋白淀粉样变性诊断
参考文献
[1] 北京医学会罕见病分会.转甲状腺素蛋白淀粉样变性多发性神经病的诊治共识.中华神经科杂志,2021,54(8):772-778.
[2] ADAMS D, ANDO Y, BEIRÃO JM, et al. Expert consensus recommendations to improve diagnosis of ATTR amyloidosis with polyneuropathy. J Neurol, 2021,268(6):2109-2122.
[3] 中华医学会心血管病学分会心力衰竭学组,中华心血管病杂志编辑委员会.转甲状腺素蛋白心脏淀粉样变诊断与治疗中国专家共识.中华心血管病杂志, 2021, 49(4):324-332.
[4] 田庄,张抒扬.《转甲状腺素蛋白心脏淀粉样变诊断与治疗中国专家共识》解读及诊断路径更新.罕见病研究,2023,2(1):63-69.
[5] 中华医学会核医学分会心脏学组,国家核医学专业质控中心. 99Tc m-焦膦酸盐单光子显像诊断转甲状腺素蛋白相关心脏淀粉样变的技术操作规范.中华核医学与分子影像杂志,2022,42(3):165-171.
[6] GILLMORE JD, DAMY T, FONTANA M, et al. A new staging system for cardiac transthyretin amyloidosis. Eur Heart J,2018,39(30):2799-2806.
[7] TSOI MR, LIN JH, PATEL AR. Emerging therapies for transthyretin amyloidosis. Curr Oncol Rep,2023,25(6):549-558.
[8] GILLMORE JD, JUDGE DP, CAPPELLI F, et al. Efficacy and safety of acoramidis in transthyretin amyloid cardiomyopathy. N Engl J Med,2024,390(2):132-142.
[9]Fontana M, Berk JL, Gillmore JD, Witteles RM, et al. Vutrisiran in Patients with Transthyretin Amyloidosis with Cardiomyopathy. N Engl J Med. 2025 ;392(1):33-44.


