198、腱鞘巨细胞瘤/色素沉着绒毛结节性滑膜炎
罕见病诊疗指南(2025年版)
概述 腱鞘巨细胞瘤(tenosynovial giant cell tumors,TGCT),也称色素沉着绒毛结节性滑膜炎(pigmented villonodular tenosynovitis,PVNS),是一种主要影响滑膜、滑囊及腱鞘的增生性炎症性疾病,可分为弥漫型和局限型。弥漫型在滑膜层上形成众多结节,常发生在如膝、踝或髋等较大的关节;而局限型则通常为单一结节,特别是在手和脚的关节或肌腱鞘处。腱鞘巨细胞瘤的特点是其在特定的关节或肌腱鞘区域的增长,可能会对受影响的部位的功能产生影响。
病因和流行病学
腱鞘巨细胞瘤的发病机制仍有争议。早期观点认为其起源于炎症反应,但后来的遗传学研究揭示了染色体改变,表明这是一种克隆性肿瘤过程。2006年的研究发现了与TGCT患者相关的常见易位,涉及1p11-13区域,该区域包含了CSF1基因,使得对该疾病的发病机制有了更深的认识。CSF1是巨噬细胞集落刺激因子(M-CSF)的另一名称,通过与其受体(CSF1R)结合,调控巨噬细胞及其前体的存活、增殖、分化和功能。在TGCT中,大多数细胞表达CSF1R,而CSF1(CSF1R的配体)只在一小部分细胞中存在(2%~16%)。易位导致肿瘤性细胞产生更多CSF1,导致更多肿瘤性细胞增加(自分泌循环),并积累非肿瘤性巨噬细胞系细胞,形成所谓的景观效应。CSF1最常见的易位伙伴是COL6A3,位于2p37染色体,导致t(1;2)(p13;p37)。然而,最近的研究表明,这种融合仅在部分患者中存在,还有其他融合伙伴导致CSF1上调。新的融合导致CSF1外显子9缺失,这是CSF1表达的负调控因子,而不是通过启动子交换导致CSF1完全过表达。
腱鞘巨细胞瘤属于罕见病,局限型是腱鞘巨细胞瘤中最常见的亚型,年发病率约为10/100万,这种肿瘤可以在任何年龄发生,但通常出现在30~50岁之间。女性患病大约是男性的两倍。弥漫型年发病率约为4/100万,往往比局限型的患者更年轻。患者的年龄分布很广,但大多数病变影响的是年轻成人,年龄小于40岁。同局限型类似,也呈现出女性发病率高的倾向。
临床表现
腱鞘巨细胞瘤的临床表现个体可有所不同,手足部位的局限型腱鞘巨细胞瘤早期常表现为无痛性包块,弥漫型腱鞘巨细胞瘤常见的症状有:肿胀、包块、僵硬及关节活动范围受限,以及疼痛。其他一些功能性的症状包括关节不稳和关节绞索等。由于这些症状的非特异性,可能导致诊断被延迟,患者需要多次就诊才最终被确诊。
此外,患者经常反映其生活质量受到影响,日常活动受到干扰,有时甚至导致无法工作,这种疾病对生活质量的影响,以及对医疗系统带来的负担,都凸显了制定合适治疗策略的重要性。
辅助检查
磁共振成像(MRI)是检查和诊断弥漫型腱鞘巨细胞瘤的首选影像。超声常用于手足部位的局限型腱鞘巨细胞瘤诊断,常规X射线检查不能确诊TGCT,但仍需检查作为鉴别诊断。
建议MRI检查方案包括T1加权、T2加权、T1增强抑脂、T2抑脂以及GRE序列。选择主要成像平面(矢状位或冠状位)取决于瘤体的具体位置。对于膝盖、踝关节和肘关节等部位,优先选择矢状位图像,而对于手部、足部、肩部、髋部和腕部等部位,则更适合冠状位图像。除非存在金属伪影,否则在成像中优先选择脂肪抑制技术。虽然梯度回波成像不在常规软组织成像方案中,但应进行T2加权成像以展示含铁血黄素情况。建议使用钆造影剂,并进行前后对比的T1加权图像减法运算。在考虑非手术治疗的情况下,可以进行动态造影增强研究以评估病变的血管化。需要以相同方式进行基线和随访检查。虽然TGCT在FDG-PET中呈高代谢,但目前还没有足够的证据支持常规进行PET-CT或PET-MR检查。
诊断
腱鞘巨细胞瘤的诊断是在临床和影像学诊断的基础上进行穿刺/切除活检病理组织学确诊。
腱鞘巨细胞瘤的病理诊断通常基于显微镜下的组织学特征。其显微镜下的外观因单核细胞、多核巨细胞、泡沫样巨噬细胞、炎症细胞、血红蛋白沉着以及基质胶原化程度的比例而异。单核细胞组分中可以识别两种主要细胞类型:小型组织细胞样细胞,具有淡色胞质和圆形或肾形核,以及较大的上皮样细胞,具有淡染胞质和圆形细胞核。
局部型腱鞘巨细胞瘤通常是分叶状且边界清晰的。类似破骨细胞的巨细胞通常很容易识别,但在某些肿瘤中可能不明显。弥漫型腱鞘巨细胞瘤具有浸润性生长,呈扩张性片状分布。类似破骨细胞的巨细胞在弥漫型中较局部型较少见。
鉴别诊断
常见的需要与腱鞘巨细胞瘤鉴别诊断的疾病包括:
1.痛风 可以出现为关节内和关节外或关节周围的结节。典型的位置,如皮下脂肪或股四头肌的远端或髌骨近端的肌腱,可以帮助区分痛风与TGCT。痛风和淀粉样变性在T2序列上呈低信号,可能是关节内的,模仿TGCT。放射学检查可能有助于评估软组织的钙化,而双能量计算机断层扫描(CT)可以用于证明痛风中单钠尿酸晶体的存在。显微镜下可见多结节状双折光性结晶,结晶周围见栅栏状组织细胞和异物巨细胞增生。
2.滑膜软骨瘤病 可以呈现为多个大小和形状相似的游离圆形体,形成“雪花”或“鹅卵石”图案,并伴有不同程度的钙化。镜下显示游离体为软骨组织伴/不伴骨化,游离体周围可见滑膜组织增生。约50%的病例出现FN1-ACVR2A和ACRVR2A-FN1基因融合。
3.树枝状脂肪瘤(lipoma arborescens) 是一种慢性、生长缓慢的关节内病变,以滑膜绒毛增生和滑膜下结缔组织被成熟脂肪细胞替代为特征。如果在去脂水平的液体敏感序列中遇到,可能会误诊为TGCT。然而,其在矢状MRI图像上的羽毛状滑膜下脂肪沉积特征是其识别特点。
4.滑膜血管瘤 可能会在关节内引起反复的自发性出血,从而在临床上类似弥漫型TGCT。然而,MRI的外观呈现出由蛇形血管通道引起的“一团蚯蚓”,并且在血管瘤中存在交替的脂肪,这有助于区分这两种情况。此外,增强模式不同,动态对比序列可用于确定滑膜血管瘤中的缓慢流动与高流动血流。显微镜下常见滑膜组织中弥漫性血管增生。
5.血友病性关节病 由于广泛的血红蛋白沉积和常伴有严重的继发性骨关节炎而类似于弥漫型腱鞘巨细胞瘤(D-TGCT),但临床史通常较为明确,并且由于没有泡沫细胞的存在,脂质成分通常是不存在的。
治疗
1.腱鞘巨细胞瘤的治疗决策需要在可能的治疗效果、患者个体的疾病自然病程、完全切除后局部复发的风险以及手术相关的并发症发生率之间取得平衡。决定采取积极治疗还是选择主动观察(active surveillance)前应该与患者共同讨论,充分评估治疗的风险和益处比例。对于没有症状的患者,应优先考虑主动观察。对于有症状的患者,如果手术或药物治疗可能导致重大并发症(例如,截肢、慢性肝炎或先前治疗出现严重毒性反应的病史),也应考虑主动观察。在选择主动观察时,随访频率应根据肿瘤生长模式、部位和症状的不同情况来个体化确定。
2.腱鞘巨细胞瘤(TGCT)的外科治疗方法依赖于关节受累的程度。对于局限型TGCT,它具有明确而清晰的边界,一般建议手术完全切除。
3.弥漫型TGCT的切除更具挑战性,因为它没有明确的边界,局部复发率可达14%~55%,而且完全滑膜切除可能会伴随术后并发症,如关节僵硬、关节功能丧失以及继发性骨关节炎,凸显了侵袭性手术所伴随的疾病负担和功能丧失。
4.腱鞘巨细胞瘤(TGCT)的系统治疗需要谨慎考虑潜在益处和副作用,同时还要评估其对生活质量的影响。治疗决策应基于症状、功能状态的变化以及疾病的解剖位置等因素。对于无症状病例,主动观察通常是首选方法,但在某些生命威胁性的情况下可能需要系统治疗。对于有症状的患者,主动观察仍然可以考虑,但需与患者沟通疾病进展可能会影响肢体远期功能。对于难以管理的症状严重的患者,如果手术可能带来明显的并发症,系统治疗可能是一个选择。需要注意的是,传统的化疗通常不适用于TGCT。
5.系统治疗的选择包括CSF1R抑制剂等药物,据报道,系统治疗药物已在TGCT中表现出一定的疗效,但治疗决策需要个体化,考虑多种因素,包括症状、疾病进展和生活质量等多个因素。目前我国尚无批准的系统治疗药物,参加国家注册临床试验是可行的选择。
6.放射治疗是弥漫型腱鞘巨细胞瘤的一种潜在治疗选项。有一项针对个体患者的荟萃分析报告了围手术期放射治疗可以降低弥漫型TGCT(D-TGCT)的复发率,但因为其长期副作用包括关节僵硬、组织坏死、皮肤反应、病理性骨折等而应用很少。此外,现在有系统疗法可供选择,具有相对更可接受的副作用,进一步限制了放射治疗的应用。因此,放射治疗不是常规选择,而是保留给有复发疾病、有症状残余疾病或无法进行保肢治疗的患者。
并发症监测
腱鞘巨细胞瘤需要进行随访和并发症监测。疾病本身可能引发关节破坏、疼痛、肿胀、运动受限等症状。手术治疗可能导致关节损伤,这些症状大约在50%的患者中持续存在。长期系统治疗可能伴随着药物相关的毒性。腱鞘巨细胞瘤长期可能会显著影响生活质量、日常活动、运动和工作,可能需要更改职业或提前退休。患者缺乏应对与疾病和护理相关的情感、心理和经济问题的帮助。患者报告的结果(PRO)数据是治疗决策的重要参考,应使用疼痛-僵硬的视觉模拟量表或数字评分量表以及PRO测量信息系统-身体功能(PROMIS-PF)问卷来评估TGCT相关症状。治疗过程中需要疼痛管理,并始终进行多学科评估。对于腱鞘巨细胞瘤的最佳随访频率,目前尚无明确数据,一般建议每年1~2次,首选磁共振成像检查。
诊疗流程(图77-1)
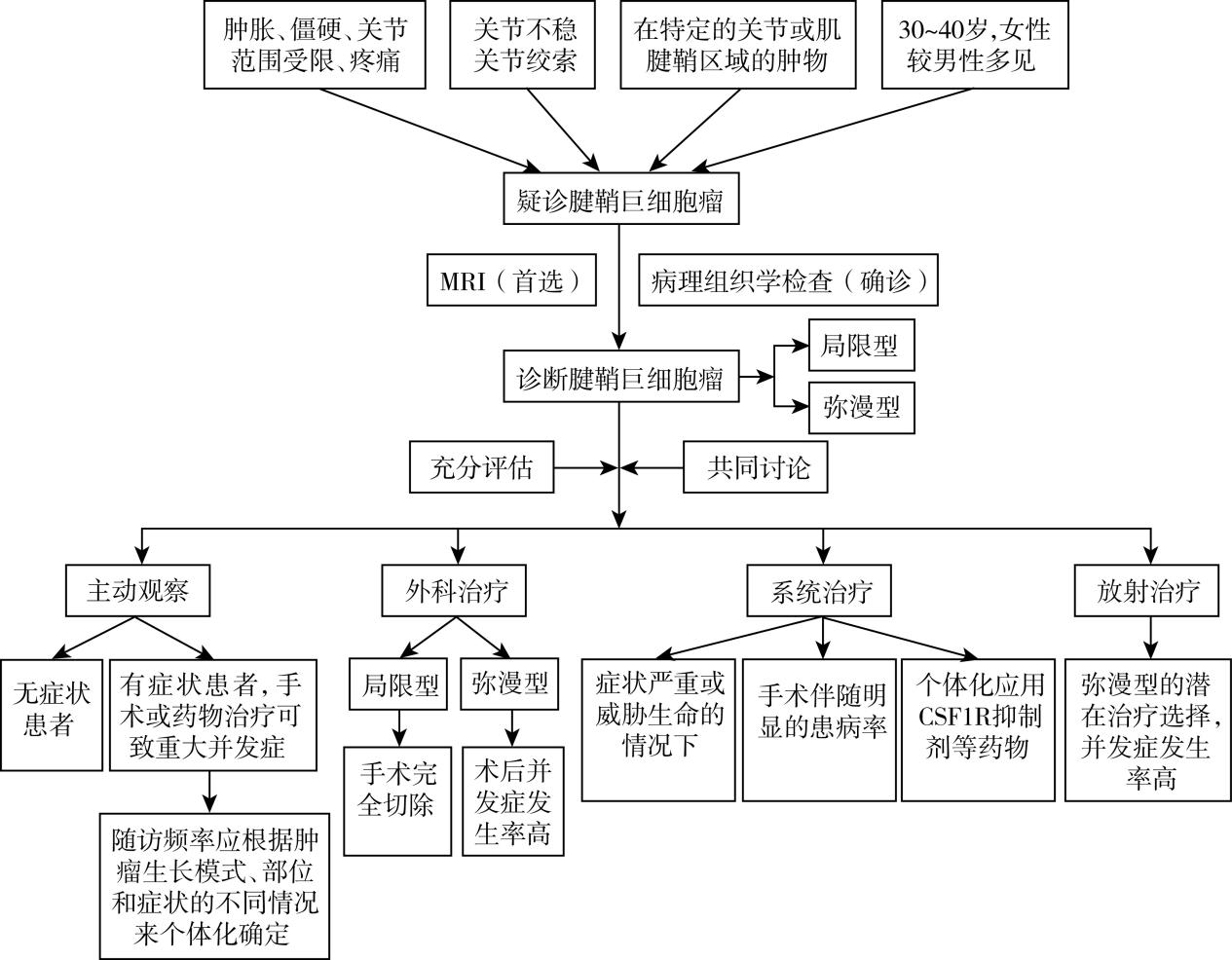
图77-1 腱鞘巨细胞瘤诊疗流程
参考文献
[1] Mastboom MJL, Verspoor FGM, Verschoor AJ, et al. Higher incidence rates than previously known in tenosynovial giant cell tumours. Acta Orthop, 2017,88: 688–694.
[2] Cupp JS, Miller MA, Montgomery KD, et al. Translocation and expression of CSF1 in pigmented villonodular synovitis, tenosynovial giant cell tumour, rheumatoid arthtritis and other reactive synovitis. Am J Surg Pathol, 2007,31:970–976.
[3] Brahmi M, Alberti L, Tirode F, et al. Complete response to CSF1R inhibitor in a translocation variant of teno-synovial giant cell tumor without genomic alteration of the CSF1 gene. Ann Oncol, 2018,29:1488–1489.
[4] Ho J, Peters T, Dickson BC, et al. Detection of CSF1 rearrangements deleting the 3’UTR in tenosynovial giant cell tumors. Genes Chromosomes Cancer, 2020,59: 96–105.
[5] Tsuda Y, Hirata M, Katayama K, et al. Massively parallel sequencing of tenosynovial giant cell tumors reveals novel CSF1 fusion transcripts and novel somatic CBL mutations. Int J Cancer, 2019,14:3276–3284.


