多学科病例讨论 | 多学科会诊综合诊治骨膜增生厚皮症1例
中国罕见病联盟
患者男性,20岁,因“面部瘢痕、下肢肿胀8年,头皮增厚4年”就诊于北京协和医院皮肤科。专科查体示面部、耳后可见多发瘢痕样增生,额部、颊部可见皱褶,睫毛粗长,上睑下垂。头皮可见条索状沟回。双下肢皮肤肿胀,双膝关节、踝关节为著。手掌、足底皮肤角化增厚。辅助检查:骨关节X线提示双手近中节指骨、掌骨、尺桡骨远端、双侧胫腓骨、股骨远端、双足跖骨骨膜增生;基因检测提示SLCO2A1基因c.1658T>A、c.96+4A>C两处变异。经多学科会诊,诊断为骨膜增生厚皮症,予口服COX-2抑制剂依托考昔治疗。
1病历简介
患者男性,20岁,因“面部瘢痕、下肢肿胀8年,头皮增厚4年”于2023年9月首诊于北京协和医院(以下简称我院)皮肤科。2024年2月22日进行多学科会诊。
1.1 现病史
患者2015年开始无明显诱因面部反复出现红丘疹、脓疱、囊肿,后形成瘢痕、皮肤增厚,同时出现双下肢肿胀,膝关节、踝关节为著,自述触之稍硬,行走后易疲累,无明显疼痛。2017年因“过敏性紫癜”曾行右下肢皮肤活检,病理提示鳞状上皮角化过度,表皮内局灶炎细胞浸润,真皮浅层小血管周围少量淋巴细胞浸润,附属器周围间质轻度黏液变性;同时发现膝关节腔及髌上囊积液、滑膜炎。 2018年开始,患者头皮逐渐增厚呈沟回状,无明显自觉症状,无脱发、头皮红丘疹等。外院考虑滑膜炎-痤疮-脓疱病-骨肥厚-骨髓炎(synovitis, acne, pustulosis, hyperostosis osteomyelitis,SAPHO)综合征,予环孢素(CsA) 50 mg bid,间断口服异维A酸(剂量不详),疗效不明显。2019年于当地医院住院治疗,完善血常规: 白细胞计数(WBC)11.0×109/L,中性粒细胞比例(NEUT%)0.804,血红蛋白(HGB)114 g/L,血小板计数(PLT)361×109/L。尿常规:蛋白、潜血(-);24 h尿蛋白:0.88→0.3→0.24 g/24 h。便常规、凝血(-)。肝肾功:白蛋白(ALB)31.7 g/L,K 3.43 mmol/L,血肌酐(Cr)32 μmol/L;炎症免疫:C反应蛋白(CRP)26.4 mg/L,红细胞沉降率(ESR)49 mm/h。抗核抗体谱、抗环瓜氨酸肽抗体(抗CCP)、类风湿因子(RF)、人类白细胞抗原B27(HLA-B27)、抗链球菌溶血素O(ASO)、白细胞介素-6(IL-6)、甲状腺功能5项、甲状旁腺素(-)。完善心电图、胸片、腹部彩超、肾脏及肾上腺彩超(-);膝关节MRI:右膝内侧半月板损伤,内侧副韧带及双侧支持带损伤,髌上囊及关节腔积液,关节软组织周围水肿;骨代谢:四肢骨盐代谢弥漫性升高,考虑骨代谢改变(图1);完善家系基因检测,检出SLCO2A1基因上c.1658T>A、c.96+4A>C两处可疑致病变异。注射用重组人Ⅱ型肿瘤坏死因子受体抗体融合蛋白(肿瘤坏死因子-α拮抗剂)25 mg 皮下注射,每周2次,MP 2 mg 口服 qd(减停),CsA 50 mg bid(减停),异维A酸 20 mg qd,米诺环素、克拉霉素抗感染等。面部囊肿稍好转出院。后长期风湿免疫科随诊。2022年期间注射用重组人Ⅱ型肿瘤坏死因子受体抗体融合蛋白联合甲氨蝶呤10mg qw,治疗后关节肿胀稍好转,2023年初停用甲氨蝶呤,加用托法替布 5 mg bid,病情稳定,炎症指标下降至正常范围内。2023年8月就诊于外院,停用注射用重组人Ⅱ型肿瘤坏死因子受体抗体融合蛋白、托法替布,建议手术治疗面部皮损,因顾虑风险未行手术治疗。2023年9月就诊于我院皮肤科,家系基因检测检出前次相同变异,诊断为骨膜增生厚皮症。患者因头皮瘙痒,自行加用托法替布5 mg bid,瘙痒好转。2023年11月就诊于我院骨科,考虑膝、踝关节肿胀,滑膜增生明显,评估后建议可行关节镜清理。于整形外科就诊,面部瘢痕可行手术治疗。2024年2月再次骨科就诊,加用迈之灵300 mg bid,建议少负重、注意保暖,加强下肢肌力锻炼。为进一步诊治,于2024年2月22日进行多学科会诊。
1.2既往史、个人史、家族史
2017年因反复下肢充血性皮疹,外院考虑过敏性紫癜、因多次复查尿潜血±、24 h尿蛋白异常,肾脏超声无殊,考虑紫癜性肾炎。同时查低钾血症逐渐加重,口服补钾中,肾内科随诊。否认药敏史。个人史无殊;父亲、母亲、姐姐均无类似表现。
1.3查体
面部、耳后可见多发瘢痕样增厚,额部、颊部可见皱褶,睫毛粗长,上睑下垂。头皮可见条索状沟回。双下肢皮肤肿胀伴色素沉着,双膝关节、踝关节肿胀明显,压痛(-),膝关节周围可见皮下脂肪断裂纹;双小腿伸侧褐色斑,融合成片。手掌、足底皮肤角化增厚(图1)。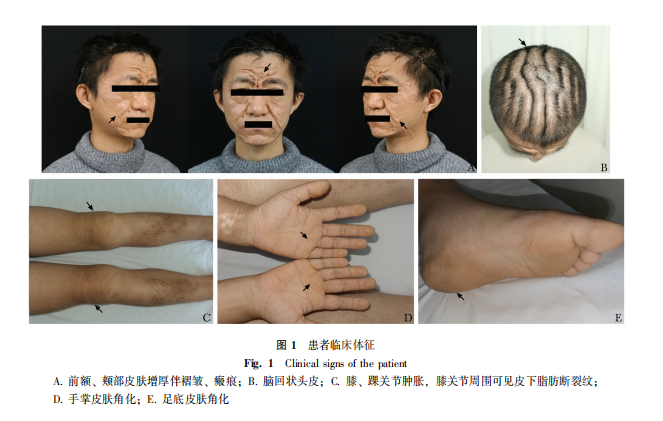
1.4辅助检查
实验室检查(2023年10月外院):WBC 9.51×109/L, HGB 121 g/L,PLT 306×109/L;肝肾功:K2.75 mmol/L(3.5~5.5 mmol/L),余大致正常范围内;炎症指标:CRP 16.71 mg/L,ESR 57 mm/h;尿常规:蛋白(-),红细胞(RBC)73/μL;甲功五项(-)。(2024年2月22日我院)尿常规+沉渣:蛋白(-),尿隐血(BLD)80 cells/μL,RBC 41.3/μL,Ab.RBC 0.2;动脉血气分析:7.42/39/107/25.3,K 2.7 mmol/L, Ca 1.11 mmol/L;尿白蛋白/肌酐比:20 mg/g;尿总蛋白/肌酐比131 mg/g。
超声(2024年2月我院):双肾未见明显异常;双侧膝关节滑膜增厚,周边软组织增厚伴关节腔积液;双侧跗骨表面不规整。
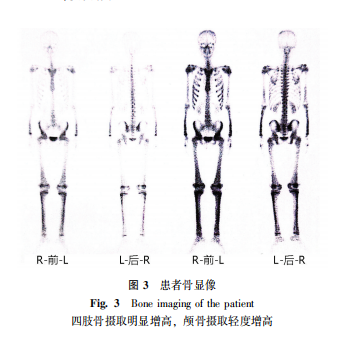
影像学检查(2024年2月我院):全脊柱正侧位:腰椎稍侧弯;双手正斜位:双侧1~3掌骨干略增粗;膝关节正侧位+髌骨轴位+胫腓骨正侧位:双侧股骨下段及胫腓骨上段骨皮质增厚、毛糙,可符合原发性肥厚性骨关节病表现。踝关节正侧位:双踝关节骨质改变符合原发性肥厚性骨关节病表现(图2)。左膝关节MRI:左侧膝关节关节腔内及髌上囊积液,滑膜皱襞增厚;左侧膝关节内、外侧半月板前后角变性;左侧膝关节侧副韧带损伤可能;左侧膝关节组成骨内多发片状质子密度高信号,红骨髓转化可能;左侧膝关节内侧软组织水肿。外院骨代谢可见四肢骨摄取明显增高,脊柱明显增高,放射分布均匀,颅骨摄取轻度增高(图3)。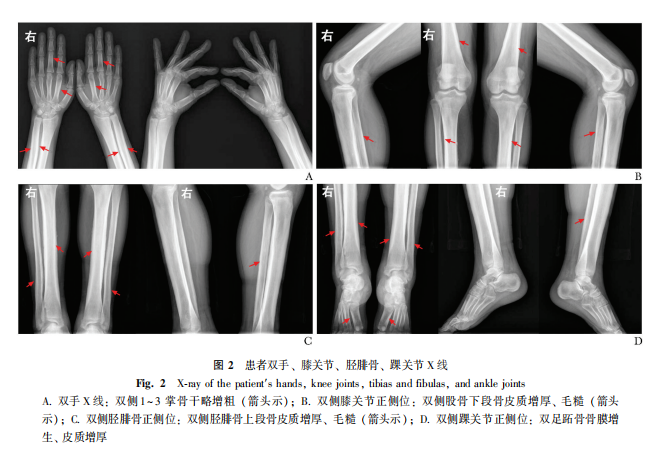
皮肤病理:患者于2017年行右小腿皮肤活检术,病理提示角质层增厚,角栓形成,棘层增厚。毛囊等附属器肥大。真皮浅层胶原明显增生,胶原间隙增宽,似有黏蛋白沉积。真皮浅中层血管周围和附属器周围可见少量淋巴组织细胞浸润,中下层真皮内汗腺丰富,汗腺周围可见黏液样物质沉积(图4)。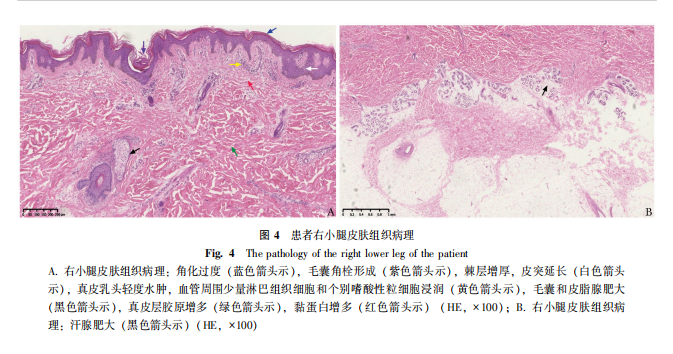
全外显子组测序:检出SLCO2A1基因上c.1658T>A、c.96+4A>C两处可疑致病变异。其中c.1658T>A变异来自母亲,c.96+4A>C变异来自父亲。姐姐亦有c.96+4A>C变异,但无c.1658T>A变异(图5)。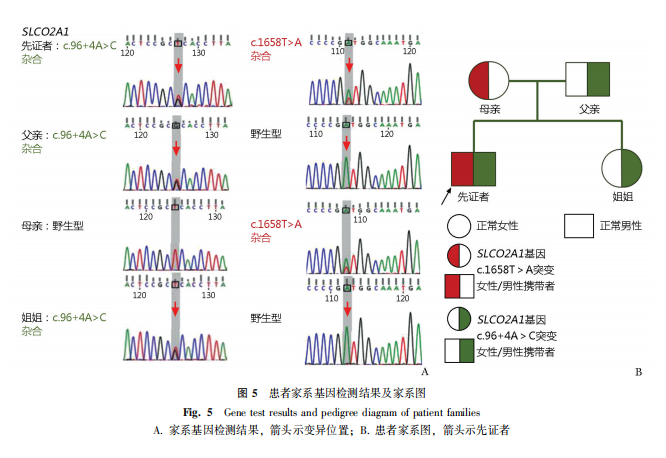
2多学科会诊讨论
2.1放射科张燕
根据患者历次骨X线结果示双手近中节指骨、掌骨、尺桡骨远端、双侧胫腓骨、股骨远端、双足跖骨骨膜增生、皮质增厚,骨干增粗,双侧对称,逐渐加重。外院MRI提示关节腔积液明显,滑膜皱襞明显增厚。考虑符合骨膜增生厚皮症改变。
2.2核医学科霍力
外院骨代谢可见四肢骨摄取明显增高,脊柱明显增高,放射分布均匀,颅骨摄取轻度增高。骨显像非病因诊断工具,根据患者骨显像表现,不符合SAPHO综合征(如胸锁关节、腰椎累及更多)骨显像改变,更符合代谢性骨病。根据患者病史,符合骨膜增生厚皮症,是否合并肾性骨病需相关科室共同评估。
2.3超声科吕珂
我院超声提示双肾未见明显异常;肠道:结肠肠壁略有增厚,结构完整。双侧膝关节、踝关节可见明显积液,尤膝关节内上侧,深度近5 cm,积液周边可见滑膜增生,厚度7~8 mm,血流信号丰富。踝关节少量积液,5 mm以内。双侧跗骨表面不规整。综上,患者肾脏、肠道无明显异常,关节积液、滑膜增生明显,病因需结合临床。
2.4皮肤科王涛
患者病理表现为角质层增厚,角栓形成,棘层增厚,毛囊等附属器肥大。真皮浅层胶原明显增生,胶原间隙增宽。真皮浅中层血管周围和附属器周围可见少量淋巴组织细胞浸润,中下层真皮内汗腺丰富,汗腺周围可见黏液样物质沉积。符合骨膜增生厚皮症表现,但病理表现不是该病诊断金标准。
2.5整形外科龙笑、夏泽楠
面部畸形是患者目前需要解决的首要问题。本例患者表现为早老面容、前额皮肤增厚伴褶皱、回状头皮、上睑下垂、睫毛粗长症、痤疮、面部瘢痕。均可考虑手术为主的综合治疗。早老面容方面:可考虑额部除皱术,中下面部除皱术、A型肉毒毒素注射等;前额皮肤增厚:直接增厚皮肤、褶皱切除术;回状头皮:头皮切除,额部提升修复或扩张器植入+头皮切除术;上睑下垂:可考虑组织减容+提肌腱膜缩短前徙;痤疮瘢痕:可予点阵激光等。由于患者皮肤增厚,张力弹性差,因此需分次手术,伤口愈合更佳。整体原则为分次手术、综合治疗和预防感染。患者全身一般状况改善、炎症指标控制,且麻醉科充分评估后,可考虑分次手术治疗。
2.6骨科吴南、徐可欣
对患者家系全外显子组测序数据进行重分析,SLCO2A1基因上检出的两处变异是有意义的、值得关注的,倾向于复合杂合的隐性遗传模式。必要时可进一步完善尿液前列腺素E2(prostaglandin E2,PGE2)检测,如后续考虑手术治疗,可完善皮肤RNA-Seq。必要时可进一步完善变异体外功能验证实验。
2.7骨科杨波
患者膝关节主要表现为滑膜炎。滑膜炎病因较多,如外伤、自身免疫性疾病、代谢性疾病等,罕见病因如厚皮厚骨膜综合征。此患者关节症状轻,关节功能可,尚不影响日常生活,可考虑保守治疗。我院膝关节MRI提示膝关节滑膜增厚,加用依托考昔后如疗效欠佳,后续可考虑关节镜清理。
2.8内分泌科夏维波
根据患者临床表现和辅助检查,考虑患者原发性肥厚性骨关节病Ⅱ型诊断基本明确,患者两处基因突变为致病突变可能性大。建议加用环氧化酶-2(cycloxidase-2,COX-2)抑制剂依托考昔60 mg qd,后续可减量维持或减停,视临床表型情况决定。本患者已20岁,后续病情倾向于稳定,依托考昔缓解症状后减停可能性大。患者合并腹泻症状,用药过程中需警惕非甾体类抗炎药的胃肠道副作用。
2.9肾内科陈丽萌、胡蓉蓉
本例患者持续镜下血尿,考虑慢性肾小球肾炎不除外,但我院尿沉渣提示以正常形态的红细胞为主,可进一步复核,此外,患者于2024年2月22日查尿蛋白阴性,建议定期检测尿蛋白变化及肾功。患者突出的、逐渐加重的低钾血症,结合患者血压不高,血气中提示碳酸氢根轻度升高,高度怀疑肾性失钾,需完善24 h尿钾佐证。SLCO2A1基因编码前列腺素转运体(prostaglandin transporter,PGT),突变引起高水平的PGE2,激活肾素-血管紧张素-醛固酮系统引起低钾血症的发生。如明确肾性失钾,本例患者建议同时完善前列腺素E代谢产物水平测定,同时进一步行基因检测分析除外其他失盐性肾病基因异常。我科既往失盐性肾病患者研究中发现这部分患者对COX抑制剂有效,因此本例患者治疗方面可考虑COX抑制剂(如吲哚美辛)等。
2.10消化内科李骥
患者病程中有腹泻症状,且SLCO2A1基因突变常有慢性肠病表现。建议完善胃肠镜、小肠重建CT明确是否有消化道受累。
2.11心理医学科洪霞
患者早期因疾病退学,目前已返学,可基本完成学业,但仍需日常佩戴口罩、帽子。追问病史时,患者与医生接触良好、对答交流可,推测原因如下:第一,患者认为医生是善意的;第二,患者反复就诊,已习惯求医过程中在医生面前的暴露。因此对于此患者目前而言,暴露疗法、训练社交技能对患者心理健康有益。
2.12血液科张炎
患者病程中曾有轻度贫血,结合患者存在前列腺素代谢障碍,临床有关节肿胀、实验室检查提示CRP等炎症指标升高,考虑既往贫血为慢性病贫血可能性大。可进一步完善血常规、网织红细胞、铁蛋白等,评估炎症水平、铁负荷等。治疗方面,以治疗原发病为主,若原发病控制不佳,贫血加重,可联合促红细胞生成素。患者目前HGB约为120 g/L,无需特殊处理。虽然文献报道本病提示有骨髓纤维化的风险,但患者临床上无脾大等明显骨髓纤维化表现,必要时可完善骨髓涂片+活检。
3诊治
诊断为骨膜增生厚皮症(原发性肥厚性骨关节病)Ⅱ型,慢性肾小球肾炎(过敏性紫癜性肾炎可能性大),低钾血症。目前患者已收入北京协和医院罕见病医学科病房,加用依托考昔60 mg qd治疗原发病,暂保留托法替布5 mg bid,炎症指标呈下降趋势;完善胃肠镜可见结肠多发充血斑,考虑SLCO2A1突变相关肠病可能;完善肾静脉彩超未见明显异常,24 h尿电解质提示肾性失钾,考虑符合SLCO2A1突变相关肾病。复查尿沉渣,潜血阳性,提示以异常形态红细胞为主,此后复查尿潜血均阴性,因此仍考虑慢性肾小球肾炎。拟待患者病情稳定后,整形外科分次行手术治疗改善面容。同时观察依托考昔对患者关节的疗效,如不理想,后续可考虑关节镜手术。
4讨论
骨膜增生厚皮症又名原发性肥厚性骨关节病(primary hypertrophic osteoarthropathy,PHO),是一种罕见的遗传病,常表现为外显不全的常染色体隐性遗传或显性遗传,也有极少的伴性遗传的报道。典型的临床症状为皮肤增厚、杵状指(趾)和骨膜增厚。2008年Uppal等[1]首次鉴定了致病基因HPGD基因(编码15-羟前列腺素脱氢酶,15-hydroxyprostaglandin dehydrogenase,15-PGDH),2012年北京协和医院首次鉴定了另一致病基因SLCOA2A1基因(编码前列腺素转运体)[2]。根据不同的基因突变,PHO分为常染色体隐性遗传1型(PHORA1,HPGD基因突变)和常染色体隐性遗传2型(PHORA2,SLCO2A1基因突变)。这两种基因突变均可导致PGE2代谢障碍,从而导致皮肤、骨骼的病理生理改变。不同分型临床表型稍有差异,PHORA1型患者常于儿童期起病,PHORA2型则多于青春期起病,更易合并消化道溃疡和骨髓纤维化,可表现为低白蛋白血症、贫血等,发病人群中男性比例远高于女性,提示性激素可能在本病的发生发展中起到调控作用[3]。
本病诊断标准为:3条主要标准,即杵状指(趾)、皮肤增厚及骨膜增生;9条次要标准,即皮脂溢出、毛囊炎、多汗、关节炎(关节痛)、指(趾)端骨质溶解、胃溃疡和(或)胃炎、植物神经综合征(如脸红、苍白)、肥厚性胃病及脑回状头皮。符合3条主要标准和数条次要标准者可诊断为完全型,符合2条主要标准和数条次要标准者为不完全型,符合1条主要标准和数条次要标准者为轻型[4]。本例患者满足皮肤增厚、骨膜增生、皮脂溢出、毛囊炎、脑回状头皮,睫毛粗长、上睑下垂(PHO表现之一[5-6]),结合患者SLCO2A1基因突变,诊断PHORA2(不完全型)明确。PHO的皮肤组织病理学可表现为皮脂腺增生、真皮水肿、黏蛋白沉积、弹力纤维变性和真皮纤维化等,因疾病分型不同,病理表现可有差异[7],本例患者小腿皮肤病理特征与文献报道相符。本例患者既往出现的贫血、低蛋白血症可能与原发病相关。
SLCO2A1基因位于染色体的3q22.1-q22.2区,编码OATP2A1蛋白,又名PGT,OATP2A1功能障碍或丧失时可导致前列腺素水平升高[2]。SLCO2A1基因突变可导致PHORA2和与SLCO2A1相关的慢性肠病(chronic enteropathy associated with SLCO2A1 gene,CEAS),这两种疾病既可同时存在,也可单独发生。Kimball等[8]对159例SLCO2A1基因突变的患者进行分析,发现60例(37.7%)为孤立的PHORA2患者,16例(10.1%)为孤立的CEAS患者,83例(52.2%)为合并PHORA2和CEAS,其中骨关节改变更常见于男性,孤立的肠道病变更多见于女性,进一步提示性激素的调控作用,但具体机制仍有待进一步阐明。本例患者检出SLCO2A1上的两处基因突变,第一处遗传自患者母亲的c.1658T>A为第12个外显子上的错义突变,既往文献无明确案例报道,但位于较为重要的结构域上,倾向于致病性,本例患者姐姐未携带该变异;第二处遗传自父亲的c.96+4A>C为基因第1个内含子区域的碱基替换,曾在两例患者中被报道[9-10],其中先证者均作为复合杂合子发病,本例患者姐姐为该变异杂合子(图5A)。因此,本团队认为患者所携带突变为复合杂合的隐性遗传模式(图5)。
PHO作为一种自限性疾病,目前尚无根治方法,主要采取对症治疗,如通过药物或手术的方式改善增厚的面部、头皮皮肤或关节症状。非甾体抗炎药可通过减少前列腺素的合成,从而达到治疗疾病的目的。据文献报道[11],COX-2抑制剂依托考昔60 mg/d 3~6个月对改善皮肤增厚、关节肿痛均有疗效。同时PHORA2患者易合并胃肠道病变,用药过程中需警惕非甾体类抗炎药的胃肠道副作用。对本例患者而言,20岁男性,已过青春发育期,后续病情倾向于稳定,依托考昔缓解症状后逐步减停可能性大。药物治疗改善美观疗效有限,因此往往需要联合整形外科手术治疗,手术设计则需“因人制宜”。早老面容、额部皱褶方面,根据沟纹深浅、增生程度不同,“多去少补”,可采用直接增厚皮肤切除术、面部除皱术或两者联合[12-13],组织量不足处,可同时行自体筋膜、真皮脂肪瓣游离移植、自体脂肪颗粒移植[14]。回状头皮方面,可考虑头皮直接切除联合额部提升修复或扩张器植入后头皮切除术[14-15]。对于上睑下垂,多采取全层楔形切除和提肌腱膜缩短前徙[6,16]。除手术外,局部注射肉毒素除皱、CO2点阵激光改善痤疮瘢痕、口服异维A酸减少油脂分泌等对症治疗也可作为辅助手段纳入治疗方案。
PHO作为一种有多系统表现的罕见遗传病,需要相关科室医师在接诊时具有足够的临床经验进行早期识别,同时,后续的治疗需要多学科合作,如皮肤科、骨科、整形外科、内分泌科和消化内科等。早期完善基因检测有助于疾病早期诊断,早期治疗,提高此类患者的生活质量。
5专家点评
皮肤科左亚刚
骨膜增生厚皮症是一种罕见的、涉及多系统受累的遗传性疾病。在本例患者的诊疗过程中,我院通过多学科诊疗模式,实现了高效、快捷的诊疗服务,赢得了患者及其家属的高度赞誉。皮肤作为人体最大的器官,往往是许多罕见病的重要临床表现部位,某些皮肤表现甚至具有特征性的诊断价值。本例患者的皮肤表现尤为特异,结合致病基因检测结果,明确了诊断,并制订了详尽的治疗方案。这一成功案例不仅为患者提供了精准的医疗服务,也为该类疾病的诊治建立了标准化的流程,具有重要的临床参考价值。
作者贡献:文章撰写:张洁;文章审阅:左亚刚、张燕、霍力、吕珂、王涛、夏泽楠、龙笑、徐可欣、吴南、杨波、夏维波、胡蓉蓉、陈丽萌、李骥、洪霞、张炎。
利益冲突:所有作者均声明不存在利益冲突。
参考文献
[1]Uppal S, Diggle CP, Carr IM, et al. Mutations in 15-hydroxyprostaglandin dehydrogenase cause primary hypertrophic osteoarthropathy[J]. Nat Genet, 2008,40(6):789-793.
[2]Zhang Z, Xia W, He J, et al. Exome sequencing identifies SLCO2A1 mutations as a cause of primary hypertrophic osteoarthropathy[J].Am J Hum Genet,2012,90(1):125-132.
[3]Li SS, He JW, Fu WZ, et al. Clinical, biochemical, and genetic features of 41 han Chinese families with primary hypertrophic osteoarthropathy, and their therapeutic response to etoricoxib: results from a six-month prospective clinical intervention[J].J Bone Miner Res,2017,32(8):1659-1666.
[4]Matucci-Cerinic M, Lotti T, Jajic I, et al. The clinical spectrum of pachydermoperiostosis (primary hypertrophic osteoarthropathy)[J].Medicine, 1991,70(3):208-214.
[5]Lu Q, Xu Y, Zhang Z, et al. Primary hypertrophic osteoarthropathy: genetics, clinical features and management[J].Front Endocrinol (Lausanne),2023,14:1235040.
[6]Ding J, Li B, Chen T, et al. Eyelid thickening and ptosis associated with pachydermoperiostosis: a case report and review of literature[J].Aesthetic Plast Surg,2013,37(2):464-467.
[7]Tanese K, Niizeki H, Seki A, et al. Pathological characterization of pachydermia in pachydermoperiostosis[J].J Dermatol,2015,42(7):710-714.
[8]Kimball TN, Rivero-García P, Barrera-Godínez A, et al. Genotype and phenotype characterization of primary hypertrophic osteoarthropathy type 2 and chronic enteropathy associated with SLCO2A1: report of two cases and literature review[J].Am J Med Genet A,2024,194(3):e63446.
[9]Huang H, Wang Y, Cao Y, et al. Interleukin-6, tumor necrosis factor-alpha and receptor activator of nuclear factor kappa ligand are elevated in hypertrophic gastric mucosa of pachydermoperiostosis[J].Sci Rep,2017,7(1):9686.
[10]Chen B. A novel compound mutation of SLCO2A1 in a Chinese patient with primary hypertrophic osteoarthropathy[J].Indian J Dermatol Venereol Leprol,2023,27:1-7.
[11]Yuan L, Liao RX, Lin YY, et al. Safety and efficacy of cyclooxygenase-2 inhibition for treatment of primary hyper-trophic osteoarthropathy: a single-arm intervention trial[J].J Orthop Translat,2019,18:109-118.
[12]刘文阁,刘玲,李素娟,等. 面部骨膜增生厚皮症的手术治疗[J].中华医学美学美容杂志,2003,9(1):41-42.
[13]刘文阁,赵继志,田华. 除皱术治疗面部骨膜增生厚皮症一例[J].中华皮肤科杂志,1999,32(6):414.
[14]Taichao D, Fuling L, Hengguang Z. Comprehensive surgical strategies for the management of pachydermoperiostosis[J].Facial Plast Surg,2018,34(3):330-334.
[15]Kara IG. Forehead lifting for cutis verticis gyrata[J].Plast Reconstr Surg,2003,111(5):1777-1778.
[16]Silva MRL, Baccega A, Duarte AF, et al. Tarsal glandular hyperplasia in pachydermoperiostosis and implications for ptosis correction[J].Ophthalmic Plast Reconstr Surg,2017,33(4):e92-e94.


