前沿 | 这些罕见病药品有望今年医保谈判;两款罕见病新药中国上市
中国罕见病联盟
2023年国家医保药品目录调整工作方案正式公布,这些罕见病药品有望谈判 6月29日,国家医疗保障局公布了《2023年国家基本医疗保险、工伤保险和生育保险药品目录调整工作方案》(以下简称《方案》)。在本次调整中,罕见病用药再次成为关注的焦点。针对罕见病治疗用药,依然不受获批时间的限制。 根据《方案》,2023年6月30日前,经国家药监部门批准上市的罕见病治疗药品,其说明书中包含《第一批罕见病目录
2023年国家医保药品目录调整工作方案正式公布,这些罕见病药品有望谈判
6月29日,国家医疗保障局公布了《2023年国家基本医疗保险、工伤保险和生育保险药品目录调整工作方案》(以下简称《方案》)。在本次调整中,罕见病用药再次成为关注的焦点。针对罕见病治疗用药,依然不受获批时间的限制。
根据《方案》,2023年6月30日前,经国家药监部门批准上市的罕见病治疗药品,其说明书中包含《第一批罕见病目录》所收录的罕见病适应证或功能主治,均可申报。这一举措扩大了谈判范围,为罕见病患者带来了更多的希望。现整理有望今年进行医保谈判的罕见病药品,如下:
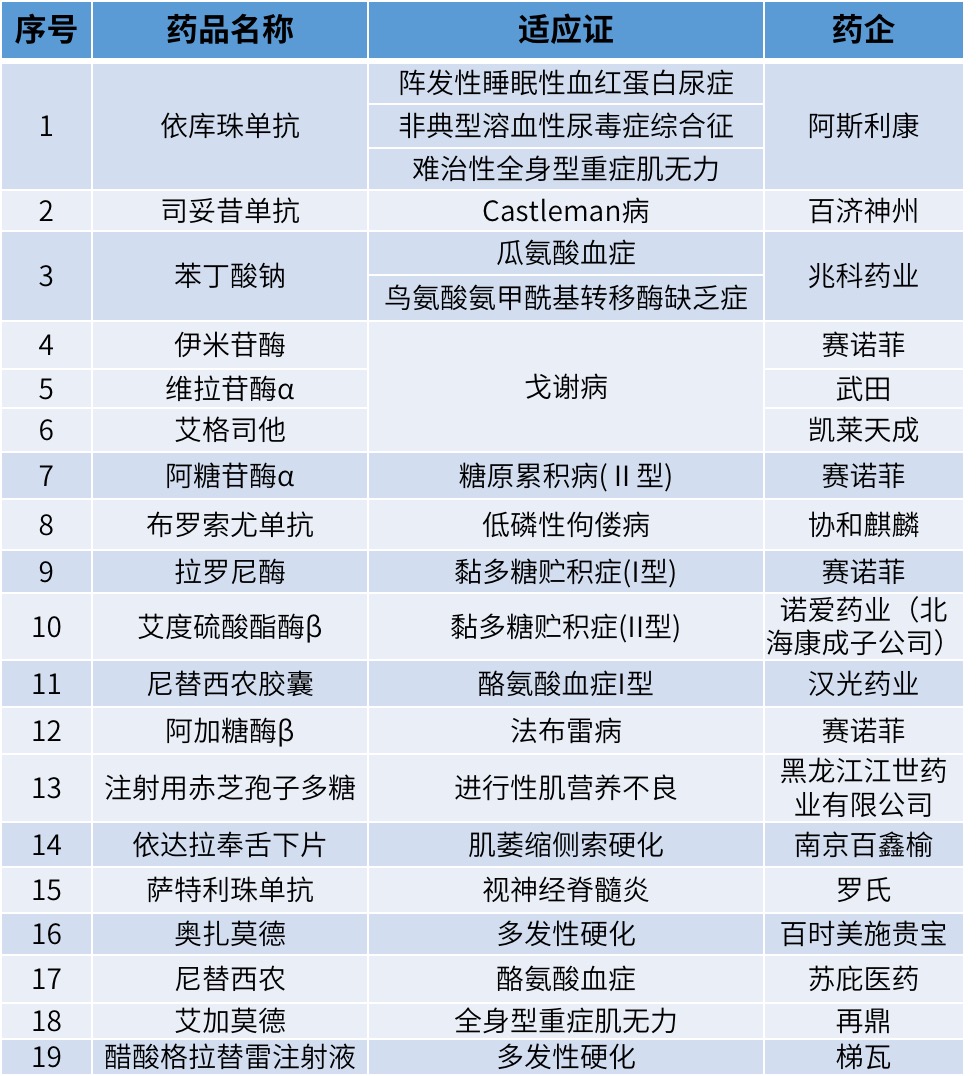
(中国罕见病联盟整理,如有不准确之处,请与我们联系)
国家药监局加速批准罕见病用药上市,改善患者治疗情况
7月5日,国务院新闻办公室就“强化药品监管,切实保障人民群众用药安全”举行发布会。宣布国家药监局将继续采取一系列措施,为罕见病患者提供新希望和机会,包括建立专门通道,优先审评境外临床急需新药,并加快审批进程。这意味着对罕见病治疗有效的药物,将获得更快的审批和上市机会,以满足患者的治疗需求。
另外,国家药监局还将提供特殊政策支持、早期介入、严审联动、全程服务和制定一系列技术指导原则,以支持罕见病新药研发。
目前这些措施已取得显著成效,已有68种罕见病用药获得批准上市。为患者提供更多治疗选择和改善疗效。国家药监局将继续加快审评审批进程,以改善罕见病患者的治疗情况。
(来源:国家药品监督管理局)
中国首个FcRn拮抗剂艾加莫德获批,用于治疗全身型重症肌无力
6月30日,艾加莫德(Efgartigimod)获国家药品监督管理局批准,成为治疗全身型重症肌无力(gMG)的新药。
重症肌无力是一种罕见的自身免疫性疾病,会导致肌肉无力和衰弱,对生命构成威胁。据估计,中国有约20万重症肌无力患者,其中85%以上会在发病后18个月内发展为全身型重症肌无力,影响全身骨骼肌肉,导致患者虚弱和过早疲劳,甚至可能影响呼吸肌肉。目前的治疗方法包括胆碱酯酶抑制剂、糖皮质激素、免疫抑制剂和静脉注射免疫球蛋白等,但仍缺乏循证医学证据支持的创新疗法。
艾加莫德是一种人源IgG1抗体的Fc片段,与新生儿Fc受体(FcRn)结合,减少致病性免疫球蛋白G(IgG)抗体并阻断IgG循环。作为首个获得批准的FcRn拮抗剂,艾加莫德已在美国、欧盟和中国用于治疗成人AChR抗体阳性的gMG,并在日本用于治疗对免疫抑制疗法无效的成人gMG。临床研究显示,艾加莫德在起效时间、疗效和安全性方面表现出出色。
艾加莫德在中国的批准对患者和临床医生来说是重要的里程碑,为他们提供了一种创新、安全、有效的疗法、有望改善患者的生活质量。
(来源:再鼎医药)
盐酸替洛利生片获批上市,成为中国首个治疗发作性睡病的创新药
6月30日,国家药品监督管理局(NMPA)正式批准盐酸替洛利生片(铧可思®)用于治疗发作性睡病(Narcolepsy)成人患者的日间过度嗜睡(EDS)或猝倒。
发作性睡病是一种罕见的睡眠/觉醒障碍疾病,临床以日间过度嗜睡(excessive daytime sleepiness,EDS)、猝倒(cataplexy)、入睡前幻觉、睡眠瘫痪和夜间睡眠紊乱为主要特征,对患者的生活质量、工作或学习能力及身心健康造成严重影响。目前我国上市的常用药物均无发作性睡病适应证,且多数为一类精神管控药品,处方管理严格,患者用药不方便,降低了药物可及性。
替洛利生是一种选择性组胺H3受体反向激动剂,在欧洲药品管理局(EMA)和美国食品药品监督管理局(FDA)分别获得了孤儿药认定,并且被FDA认定为突破性治疗药物。替洛利生是在全球范围内唯一获得发作性睡病适应证,并且同时被美国、欧洲和中国指南推荐的非精神管控类药物。这也是唯一在中国获批发作性睡病适应证的创新药。
(来源:琅钰集团)


