前沿 | 第三批适用增值税政策的抗癌药品和罕见病药品清单发布;复星医药自主研发的罕见病创新药GC101获国家药监局临床试验批准
中国罕见病联盟
第三批适用增值税政策的抗癌药品和罕见病药品清单发布 11月21日,财政部、海关总署、税务总局、药监局等四部门发布关于发布第三批适用增值税政策的抗癌药品和罕见病药品清单的公告,自2022年12月1日起,本公告中的抗癌药品和罕见病药品按照规定执行相关增值税政策。各批清单中的抗癌药品和罕见病药品制剂需已获准上市,对应剂型以国家药品监督管理部门实际批准上市剂型为准。 (来源:财政部网) 荣昌生
第三批适用增值税政策的抗癌药品和罕见病药品清单发布
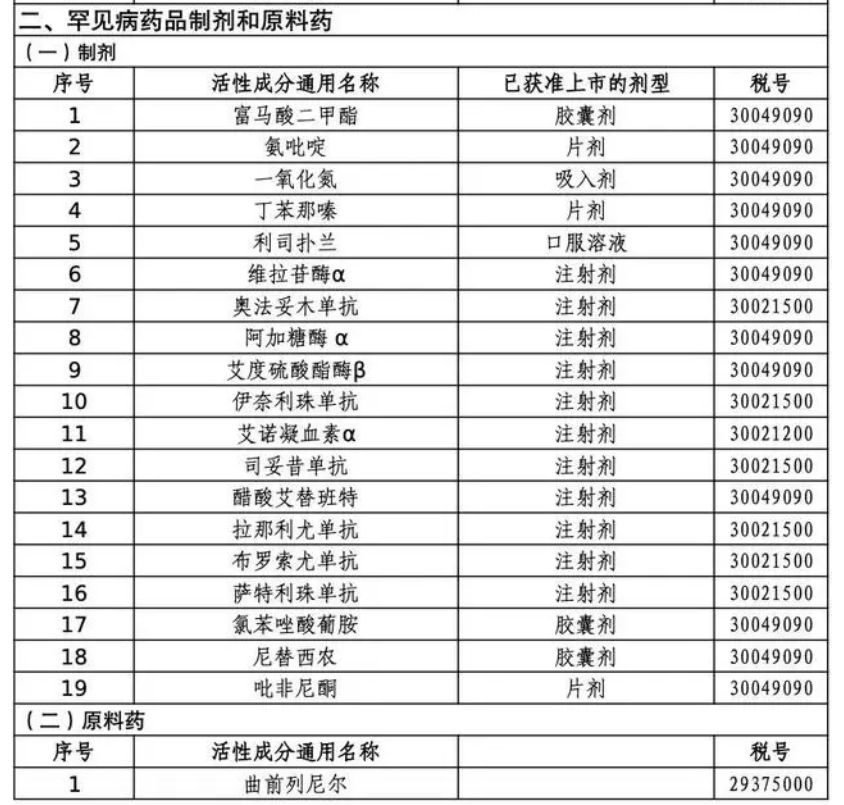
11月21日,财政部、海关总署、税务总局、药监局等四部门发布关于发布第三批适用增值税政策的抗癌药品和罕见病药品清单的公告,自2022年12月1日起,本公告中的抗癌药品和罕见病药品按照规定执行相关增值税政策。各批清单中的抗癌药品和罕见病药品制剂需已获准上市,对应剂型以国家药品监督管理部门实际批准上市剂型为准。
(来源:财政部网)
荣昌生物泰它西普再获重磅认定,针对重症肌无力
11月17日,荣昌生物制药宣布,注射用泰它西普正式被国家药监局药品审评中心(CDE)纳入突破性治疗品种,用于治疗全身型重症肌无力。此次泰它西普获CDE授予突破性治疗品种,是基于其一项治疗全身型重症肌无力的国内Ⅱ期临床研究。该项研究由北京医院许贤豪教授牵头完成,结果显示泰它西普能显著改善全身型重症肌无力患者的病情,体现出良好的有效性和安全性。2022年10月,荣昌生物宣布,泰它西普重症肌无力适应症获得美国食品药品监督管理局(FDA)颁发的孤儿药资格认定。据悉,获得认定的药物可在美国享受上市申请快速通道、上市后7年市场独占期以及税收优惠等激励政策。
(来源:荣昌生物)
复星医药自主研发的罕见病创新药GC101获国家药监局临床试验批准
2022年11月14日,上海复星医药宣布,控股子公司上海精缮生物科技有限责任公司自主研发的细胞和基因治疗产品GC101的临床试验申请于近日获国家药品监督管理局批准。该产品为1类治疗用生物制品(创新型生物制品),可用于隐性营养不良型大疱性表皮松解症(Recessive Dystrophic Epidermolysis Bullosa,RDEB)患者难以愈合的体表伤口的移植治疗,拟于条件具备后于中国境内(不包括港澳台地区)开展I期临床试验。
RDEB是一种单基因常染色体隐形遗传病,被《第一批罕见病目录》列为罕见病,患者的皮肤和眼睛、口腔、食道、呼吸道等粘膜组织在受到轻微摩擦后就会发生水疱或血疱,进而创伤溃烂,皮肤"像蝴蝶翅膀一样脆弱";因此患者常被称作“蝴蝶宝贝”。 截至目前,于全球范围内尚无同类用于RDEB治疗的产(药)品获批上市。
(来源:复星医药)
剑指重症肌无力,优时比创新疗法在美、欧上市申请获受理
近日,优时比(UCB)宣布,美国FDA与欧洲药品管理局(EMA)已分别接受其在研药物zilucoplan的新药申请(NDA)与上市许可申请(MAA)。Zilucoplan是一款经皮下给药的新型大环肽类C5补体抑制剂,用于治疗患有乙酰胆碱受体抗体阳性(AChR-Ab+)全身性重症肌无力(gMG)的成年患者。作为一种靶向疗法,zilucoplan可抑制gMG潜在病理生理学中的关键成分,设法解决神经肌肉接头损伤的潜在机制。
2019年,美国FDA授予了zilucoplan孤儿药资格,用于治疗MG。欧盟委员会于2022年授予了zilucoplan孤儿药资格,同样用于治疗MG。前不久,欧洲药品管理局(EMA)接受了zilucoplan的上市许可申请(MAA),用于治疗除了类固醇或非甾体免疫抑制剂之外还需要治疗的AChR-Ab+ gMG成年患者。
此次NDA和MAA均基于针对gMG的关键3期RAISE研究。试验达到其主要终点,使用zilucoplan治疗可在关键的MG特异性的结果方面产生具有临床意义和统计学意义的改善。
(参考资料:
[1] UCB announces U.S. FDA acceptance of new drug application and EMA MAA validation for zilucoplan for the treatment of generalized myasthenia gravis in adult patients. Retrieved November 14, 2022, from https://www.ucb.com/stories-media/Press-Releases/article/UCB-announces-US-FDA-acceptance-of-new-drug-application-and-EMA-MAA-validation-for-zilucoplan-for-the-treatment-of-generalized-myasthenia-gravis-in-adult-patients)


