203、肿瘤相关骨软化症
罕见病诊疗指南(2025年版)
概述 肿瘤相关骨软化症(tumor-induced osteomalacia,TIO),又称肿瘤性骨软化症,是获得性低磷性佝偻病的常见类型。TIO是一种由于肿瘤分泌调磷因子引起肾脏磷丢失增多造成的获得性低磷性骨软化症,是一种罕见的副肿瘤综合征。肿瘤分泌的调磷因子通常是成纤维细胞生长因子23(fibroblast growth factor 23, FGF23),其他调磷因子罕见。临床表现为骨痛、乏力,病情严重者可有病理性骨折,骨骼畸形,行动障碍等。生化特点为血磷降低,碱性磷酸酶(ALP)升高,尿磷增多,1,25(OH)2D水平相对降低。引起TIO的肿瘤多是来源于间叶组织的良性肿瘤,位于骨或软组织内,位置隐匿,生长缓慢,体积较小。肿瘤完整切除后,患者血磷水平可恢复正常,症状逐渐缓解。
病因和流行病学
TIO的起因是肿瘤产生调磷因子导致的低磷血症。肿瘤分泌的调磷因子绝大多数是FGF23,其是磷酸盐稳态的主要调节因子,作用于近端肾小管,导致肾小管磷酸盐重吸收减少。此外,FGF23抑制近端小管中1-α-羟化酶的表达,导致1,25双羟维生素D [1,25(OH)2D]水平不足,从而降低肠道磷酸盐和钙的吸收。过量FGF23的产生导致低磷血症、骨软化以及继发性甲状旁腺功能亢进症。除FGF23外,其他调磷因子,包括分泌型卷曲相关蛋白(secreted frizzled-related protein-4)、 FGF7、细胞外基质磷酸糖蛋白(matrix extracellular phosphoglycoprotein)偶尔可见报道。
导致TIO的肿瘤90%为良性,经常体积小,位置隐匿。肿瘤部位,约50%肿瘤位于下肢,25%位于头颈部。病理诊断方面,磷酸盐尿性间叶肿瘤(phosphaturic mesenchymal tumors PMTs)约占80%,血管外皮细胞瘤约占9%。其他少见肿瘤包括:良性骨肿瘤(骨化性纤维瘤、软骨间充质瘤、软骨母细胞瘤)、骨巨细胞瘤、神经鞘瘤、腱鞘巨细胞瘤、良性皮肤肿瘤(纤维组织细胞瘤、和血管平滑肌脂肪瘤)、牙源性肿瘤、肌纤维母细胞瘤、骨肉瘤、前列腺癌、软组织肉瘤、肺癌、肾脏肿瘤、乳腺肿瘤、神经内分泌肿瘤、血液系统恶性肿瘤、甲状腺乳头状肿瘤、子宫纤维瘤、黑色素瘤、胸腺类癌等。
由于除PMT之外的其他肿瘤临床上很难和低磷血症联系起来,因此TIO的真实患病率和发病率的数据难以统计。国外报道成人肿瘤性骨软化症(TIO)发病率约为1/100万,患病率约为1/23万。目前TIO的报道全球已经超过1000例,其中5%左右的病例未找到相关肿瘤。
临床表现
骨痛 以下肢痛、腰背痛或肋间痛起病,逐渐发展为全身多部位骨骼疼痛。查体时可有胸廓挤压痛、骨盆挤压痛、脊柱叩击痛等。
乏力 程度不一,包括全身无力、腿脚发软、运动减少等。
活动障碍 重症者需拄拐行走,甚至长期卧床。
病理性骨折 多发脊椎压缩骨折后,患者身高可降低,脊柱可出现畸形。肋骨、骨盆。下肢病理骨折时,可以出现相应畸形。
部分患者出现牙齿松动或脱落,严重者多颗牙齿呈片状脱落。
辅助检查
1.化验检查
(1)血磷:低磷血症。具体参考各年龄段及各医院血磷正常值。一般低磷血症为血磷<0.8 mmol/L。
(2)肾磷阈:肾小管最大磷酸盐重吸收率与肾小球滤过率的比值(TmP/GFR)<0.8 mmol/L。24小时尿磷在疾病早期升高,晚期降低。
(3)血钙、甲状旁腺素(PTH)、25-羟维生素D[25(OH)D]、1,25双羟维生素D[1,25(OH)2D]和碱性磷酸酶(ALP):血钙正常,PTH正常或轻度升高,25(OH)维生素D正常或降低。1,25双羟维生素D[1,25(OH)2D]血清水平接近正常或明显降低。血清ALP升高。
(4)血清FGF23:在低磷血症的情况下,完整的FGF23水平大于30pg/ml是诊断FGF23介导的低磷血症的重要指标,C-末端FGF23也可以作为检测指标(FGF23正常水平需参考使用的检测试剂盒)。
2.影像学检查
(1)X线检查:双手、双膝、足踝或骨盆、胸腰椎正侧位等部位X线照相,可见骨小梁纹理模糊、骨盆变形(三叶形、漏斗形等)、病理骨折(椎体压缩骨折多见)、假骨折线(耻骨、坐骨常见)、股骨头变形等。
(2)双能X线骨密度测定:腰椎及股骨近端骨密度降低。
(3)奥曲肽显像即生长抑素受体显像:将放射性核素(99mTc、68Ga、18F、111In等)标记的生长抑素类似物(多使用奥曲肽)注射入患者体内,奥曲肽与体内病灶细胞表面的特异受体相结合(PMTs多表达生长抑素受体,somatostatin receptor 2,SSTR2为主),放射性核素发射出来的γ射线被成像设备(SPECT/CT、PET/CT、PET/MR)接收,从而使肿瘤显影,帮助定位病灶。68Ga-DOTATATE PET/CT显像(68Gallium DOTATATE positron emission tomography/computed tomography)是首选的诊断和定位TIO致病肿瘤的影像诊断技术。99mTc生长抑素受体SPECT 全身显像(technetium-99m HYNIC-TOC single- photon emission computed tomography, 99mTc-HYNIC-TOC SPECT)等也是发现TIO肿瘤的有效方法。一旦功能显像发现了可疑肿瘤,解剖显像可以更精确地定位肿瘤,包括X线平片、超声、计算机断层扫描(CT)或磁共振(MR)等。
(4)18FDG PET-CT,在奥曲肽显像无法定位肿瘤时,18FDG PET-CT可能帮助发现病灶,但发现率不及奥曲肽显像。
诊断
1.临床、影像检查存在骨软化,化验检查发现存在肾磷阈下降(TmP/GFR<0.8 mmol/L)引起的低磷血症(<0.8 mmol/L),而血清钙水平正常,ALP升高;通过查体、奥曲肽显像以及彩超、CT、MRI等发现相关肿瘤,而肿瘤切除后患者血磷恢复正常即诊断为TIO。
2.血清FGF23水平在低血磷的前提下大于30pg/ml对于确诊极有帮助,但鲜有医院开展此类检测项目。
3.TIO临床表现的非特异性使得疾病的早期识别变得困难,因此文献报道中骨软化的症状在诊断前平均已存在4年。引起TIO的肿瘤通常很小,生长缓慢,几乎可位于身体的任何地方,因此定位相当具有挑战性的。奥曲肽显像大大提高了肿瘤检出效率。
4.PMTs患者多数会出现TIO。常规病理可以诊断PMTs,其多为温和的梭形细胞伴有基质沉积,粗糙钙化,和/或丰富的血管网。肿瘤组织中FGF23高表达。疑难病例可以通过分子检测FN1-FGFR1或FN1-FGF1融合基因帮助确诊。
鉴别诊断
1.TIO疼痛症状分布广泛,定位模糊,缺乏明显特异性。骨痛需要与:脊柱关节病、骨质疏松症、多发性骨髓瘤、转移性骨病、风湿性多肌痛、多发性肌炎等鉴别。
2.本病生化血磷酸盐水平表现为慢性长期降低,需要与久泻不止、长期使用利尿剂、长期服用大量含铝的抗酸剂、使用大量茶碱(治疗哮喘)等引起慢性低磷血症相鉴别。此外,还需要与以下多种疾病鉴别。
3.原发性甲状旁腺功能亢进症。由一个或多个甲状旁腺发生疾病引起PTH过多分泌所致。可导致高钙血症、低磷血症和骨吸收过多(钙从骨组织转移到血液中)。骨吸收过多进而导致骨质疏松症。
4.遗传性低磷性佝偻病,其常见类型为X连锁低磷性佝偻病是由于位于X染色体上的PHEX基因的突变,导致肾小管重吸收磷减少。肠道吸收磷不良,血磷降低,骨矿化不良。遗传方式是X染色体显性遗传,幼年起病,身材矮小、骨骼畸形,部分患者有家族史。
5.晚期慢性肾脏疾病(尤其是透析患者),经常随餐口服磷酸盐结合剂,以减少食物中磷酸盐的吸收。长期使用磷酸盐结合剂可能引起低磷血症。
治疗
1.TIO的致病肿瘤一经定位,完整切除肿瘤是最有效的治疗方案。血磷水平的正常化多数发生在手术后5天左右。血磷恢复正常的患者,术后约6个月骨痛明显缓解,骨密度明显升高。
2.骨内肿瘤无法整块完整切除时,可以考虑先刮除病灶,后通过物理或化学的方法处理骨壳,以降低复发率。术后定期复查血磷。血磷降低,提示肿瘤复发。复发肿瘤建议再次手术切除。无法切除的病灶,可以考虑影像引导下行射频消融或冷冻消融。
3.无法定位肿瘤或不能完全切除肿瘤时,常规治疗采用磷酸盐加活性维生素D(骨化三醇或阿法骨化醇)。常规药物治疗的治疗目标是缓解临床症状,升高血磷水平,使ALP恢复正常,使甲状旁腺激素(PTH)维持在正常范围内。血磷水平完全恢复正常通常代表用药过量。建议每天服用磷酸盐中元素磷含量为20~40 mg/kg(成人为1~3 g/d),骨化三醇为20~30 ng/kg(成人为0.5~1.5 µg/d)。阿法骨化醇的等效剂量为骨化三醇的1.5~2倍。磷酸盐补充剂应每天分4~6次口服,并在数周内逐渐调整至目标剂量。每3~6个月监测一次肾功能、血清钙、磷、ALP、PTH和24 h尿钙水平,以调整药物剂量,预防继发性或三发性甲状旁腺功能亢进、肾结石和肾功能下降等并发症。未能定位肿瘤患者,需要定期(每1~2年)重复定位肿瘤的影像检查。
4.布罗索尤单抗(burosumab)是针对FGF23的全人源性IgG1单克隆抗体,已在我国被批准用于成人和1岁及以上儿童患者的X连锁低磷血症(XLH)和成人无法根治性切除或定位的TIO的治疗。由于布罗索尤单抗不能阻止致病肿瘤的进展或生长,它的使用应仅限于肿瘤无法切除或无法定位的患者。成人TIO研究证实,布罗索尤单抗可改善磷调节和骨健康相关生化指标,改善关节僵硬、缓解疼痛、提升运动能力,促进骨折愈合。
诊疗流程(图82-1)
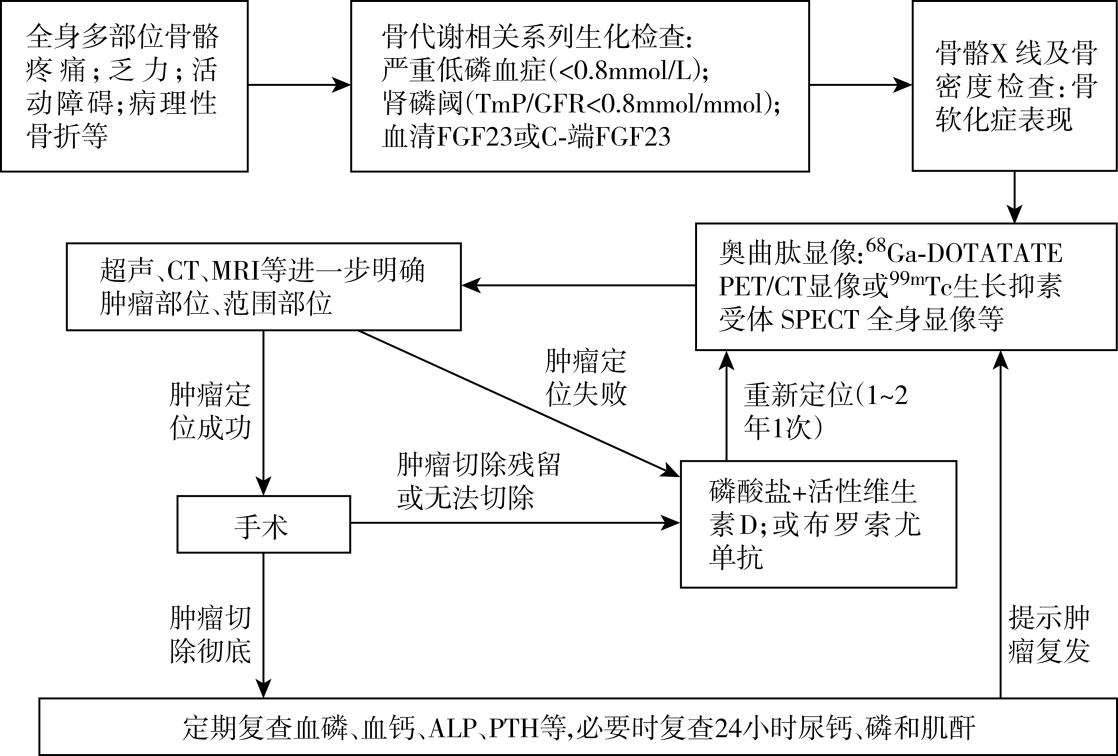
图82-1 肿瘤相关骨软化症诊疗流程
参考文献
[1] WHO CLASSIFICATION OF TUMOURS EDITORIAL BOARD. Soft tissue and bone tumours. 5th ed. Lyon, France:IARC Press, 2020.
[2] MINISOLA S, PEACOCK M, FUKUMOTO S, et al. Tumour-induced osteomalacia. Nat Rev Dis Primers,2017,3:17044.
[3] WALTON RJ, BIJVOET OL. Nomogram for derivation of renal threshold phosphate concentration. Lancet,1975,2(7929):309-310.
[4] RENDINA D, ABATE V, CACACE G, et al. Tumor-induced osteomalacia: a systematic review and individual patient's data analysis. J Clin Endocrinol Metab, 2022,14;107(8):e3428-e3436.
[5] 许志阳,李文波,黄子达,等. 12例低磷性骨软化症误诊误治临床分析.中国骨与关节杂志,2019,8(5):368-373.
[6] 庞芮.肿瘤性骨软化症的临床特点、影像学定位及SSTR2&5免疫组化分析.北京:中国医学科学院,2018.
[7] ABRAHAMSEN B, SMITH CD, MINISOLA S. Epidemiology of tumor-induced osteomalacia in Denmark. Calcif Tissue Int,2021,109(2):147-156.
JAN DE BEUR SM, MINISOLA S, XIA WB, et al. Global guidance for the recognition, diagnosis, and management of tumor-induced osteomalacia. J Intern Med. 2023,293(3):309-328.


