200、血栓性血小板减少性紫癜
罕见病诊疗指南(2025年版)
概述 血栓性血小板减少性紫癜(thrombotic thrombocytopenic purpura, TTP)是由于遗传性或获得性ADAMTS13缺乏,引起广泛微血管血栓形成,导致消耗性血小板减少、微血管病性溶血、心脑肾等重要脏器功能障碍的一种罕见的血栓性微血管病。
病因和流行病学
根据ADAMTS13缺乏机制不同,TTP分为遗传性TTP(cTTP,又称为Upshaw-Schulman综合征)和免疫性TTP(iTTP)。cTTP系ADAMTS13基因突变导致血浆ADAMTS13活性缺乏,常在感染、炎症或妊娠等诱发因素下发病。cTTP呈常染色体隐性遗传,ADATMS13基因突变类型多为纯合子型或双重杂合子型。iTTP系因患者体内产生抗ADAMTS13自身抗体,抑制ADAMTS13活性(中和抗体)或与ADAMTS13结合形成抗原抗体复合物,加速ADAMTS13在体内的清除。iTTP多无明确病因(即原发性),也可能继发于感染、药物、肿瘤、自身免疫性疾病、造血干细胞移植等。iTTP是最常见的临床类型,占TTP总病例数的95%左右;cTTP较为少见,仅占总病例数的5%,但在儿童和孕妇患者中cTTP却占到25%~50%。国外资料显示TTP年发病率(2~6)/100万,女性:男性约为2∶1。发病年龄分布以30~50岁为高峰,但部分cTTP患者在新生儿期即可发病,女性cTTP患者常在妊娠早期出现疾病发作。
临床表现
多数TTP患者发病急骤、病情危重,少数患者发病隐匿、临床表现不典型。炎症、感染、妊娠等是常见的TTP诱发原因。
临床TTP典型表现:①出血,以皮肤、黏膜为主,严重者可有内脏或颅内出血;②微血管病性溶血性贫血(MAHA)多为轻、中度贫血,可伴黄疸;③神经精神症状,表现为意识紊乱、头痛、失语、惊厥、视力障碍、谵妄、偏瘫以及局灶性感觉或运动障碍等,缺乏典型表现,以发作性、多变性为特点;④肾脏损害,可出现蛋白尿、血尿、管型尿,血尿素氮及肌酐轻度升高;⑤发热(体温>37.5 ℃)。此外,还可有其他器官损伤的临床表现,如胸痛、腹痛、乏力、关节痛、肌肉痛等症状。
临床上典型的TTP“五联征”已相对少见,而以微血管病性溶血性贫血、血小板减少和神经精神症状为主的“三联征”更为常见。由于部分TTP患者神经精神症状不显著,建议如发现微血管病性溶血性贫血和血小板减少时,就要高度警惕TTP可能,及时进行相关实验室检查和重要脏器功能评估。
辅助检查
1.血常规及血涂片检查 不同程度贫血;外周血涂片可见破碎红细胞(>1%),网织红细胞比例大多增高,可见晚幼红细胞;血小板计数显著降低,多低于20×109/L,且动态下降较显著。
2.血生化检查 主要有血胆红素升高,以间胆升高为主;血清乳酸脱氢酶(LDH)明显升高;血尿素氮及肌酐不同程度升高,肌钙蛋白T水平升高者见于心肌受损者。
3.血浆ADAMTS13活性及抑制物或IgG抗体测定 TTP患者血浆ADAMTS13活性显著降低(<10%正常混合血浆活性);iTTP患者ADAMTS13活性显著降低且检出ADAMTS13抑制物或IgG抗体;cTTP患者不存在ADAMTS13抑制物或IgG抗体,基因测序则有助于诊断。血浆ADAMTS13活性及抑制物或IgG抗体测定血样尽可能在血浆置换前留取。
4.凝血检查 APTT、PT及纤维蛋白原检测多正常,偶有纤维蛋白降解产物轻度升高。
5.溶血相关检查 红细胞直接抗人球蛋白试验阴性,但在部分继发于免疫性疾病的患者中可为阳性;血浆游离血红蛋白增加、血清结合珠蛋白下降。
6.基因检测 对怀疑cTTP患者可进行ADAMTS13基因突变检测,有助于确立诊断及遗传咨询。
7.其他 包括HBV、HCV、HIV病毒血清学检查,甲状腺功能,抗核抗体谱,狼疮抗凝物,抗磷脂抗体以及脑部CT/MRI检查,脑电图等。
诊断
1.具备TTP临床表现 如出血、微血管病性溶血性贫血、神经精神症状等。
2.典型的血细胞变化和血生化改变 血小板计数显著降低、贫血,尤其是外周血涂片中红细胞碎片>1%;血清游离血红蛋白增高,血清乳酸脱氢酶明显升高。
3.血浆ADAMTS13活性显著降低(<10%正常混合血浆活性),iTTP者常检出ADAMTS13抑制物或IgG抗体。
4.排除溶血尿毒症综合征(HUS)、弥散性血管内凝血(DIC)、HELLP综合征、Evans综合征、子痫、灾难性抗磷脂抗体综合征等疾病。
由于TTP患者临床表现存在明显个体差异,对疑似患者需进行危险度评估,推荐使用PLASMIC评分系统。积分0~4分为低危,TTP预测效率0~4%;积分5分为中危,预测效率5%~24%;积分6~7分为高危,预测效率62%~82%。对临床评估中度或高度疑似TTP患者应及时留取血样本送检ADAMTS13活性及抑制物或IgG抗体测定,不必等待检测结果即可开始相关治疗。如后续检测报告血浆ADAMTS13活性<10%,即可诊断TTP;血浆ADAMTS13活性>20%者可基本排除TTP;血浆ADAMTS13活性介于10%~20%之间者并不能完全排除TTP,需根据临床判断及随访。
鉴别诊断
1.溶血尿毒症综合征(HUS) 分为典型的HUS和补体介导的不典型HUS(aHUS),前者主要由产志贺毒素的大肠埃希菌感染导致。后者与补体活化替代途径加速激活相关。患者具有溶血性贫血、血小板减少和肾功能损害3个基本特点。HUS患者肾功能损害更严重,而神经系统症状较轻。患者血浆ADAMTS13活性正常或仅轻度降低。
2.弥散性血管内凝血(DIC) 多继发于严重感染、创伤、肿瘤或病理产科,DIC主要病理过程为凝血酶和纤溶酶的异常激活,导致凝血功能的显著异常。临床上出血表现突出,除了由血小板减少外,APTT、PT延长,纤维蛋白原显著降低、D-D聚体或FDP明显增高。因此血凝常规异常有助于DIC诊断。
3.HELLP综合征 是指以微血管病溶血性贫血、转氨酶升高和血小板计数降低为特征的综合征,多发生于妊娠中晚期妇女。患者血浆ADAMTS13活性正常或仅轻度降低。HELLP症状和体征可在分娩后缓解。
4.子痫 是指子痫前期或妊娠期高血压患者新发全身性强直-阵挛性抽搐或昏迷,通常发生于妊娠晚期,分娩后缓解。75%的患者伴有血压增高,血液学改变较轻,血小板一般不低于20×109/L。患者血浆ADAMTS13活性正常或仅轻度降低。
5.Evans综合征 具有自身免疫性溶血性贫血和免疫性血小板减少引起的临床表现。但患者外周血涂片无破碎红细胞,无神经系统异常等脏器损害特点。患者血浆ADAMTS13活性正常或仅轻度降低。患者抗人球蛋白试验阳性,而TTP患者一般抗人球蛋白试验阴性。
6.灾难性抗磷脂抗体综合征(CAPS) 是一种危及生命的罕见抗磷脂综合征,常累及全身大、小血管造成严重血栓形成并发症,多个器官同时或短期内相继受累。CAPS患者至少间隔12周两次检出狼疮抗凝物、抗β2-糖蛋白1抗体和/或抗心磷脂抗体阳性。患者血浆ADAMTS13活性正常或仅轻度降低。
治疗
1.治疗原则 本病多急性发病,如不能及时治疗死亡率高。临床上在中度或高度怀疑本病时即应尽快开始相关治疗。iTTP首选血浆置换治疗,并酌情联合使用肾上腺皮质激素等。cTTP以替代治疗为主,分为按需治疗和预防治疗方法。对高度疑似和确诊病例输注血小板应十分谨慎,血浆置换后如出现危及生命的严重出血时才考虑使用。
2.治疗方法
(1)治疗性血浆置换:适用于确诊的iTTP治疗和临床中/高度怀疑TTP的初始紧急治疗。血浆置换采用新鲜(冰冻)血浆,血浆置换量推荐为2000~3000ml/次,每日1~2次,直至症状缓解、血小板计数恢复正常连续2天后可逐渐延长血浆置换间隔直至停止。当肾功能衰竭时,可与血液透析联合应用。血浆置换通过清除血液中ADAMTS13抑制物或IgG抗体及其他致病因素、补充新的ADAMTS13而发挥作用。患者对血浆置换的治疗反应差异较大,对连续血浆置换治疗5次仍未取得临床反应的患者仍建议继续血浆置换治疗,同时还应积极寻找诱因(如感染等)并加以祛除。对确无条件血浆置换者,可暂输注新鲜(冰冻)血浆,剂量为每日20~40ml/kg,注意液体量平衡。
(2)肾上腺皮质激素:肾上腺皮质激素可减轻炎症反应、保护器官功能、抑制自身抗体产生。主要适用于iTTP治疗。可选用甲基泼尼松龙(80~120mg/d)或地塞米松(15~20mg/d)静脉输注,病情缓解后可过渡至泼尼松[1~2mg/(kg·d)],并减量至停用。肾上腺皮质激素使用要考虑到其对内分泌、心血管和神经精神方面的副作用,对原有高血压、糖尿病、老年及精神疾病者使用肾上腺皮质激素要特别关注药物的不良反应。
(3)利妥昔单抗:通过选择性耗竭B淋巴细胞,降低ADAMTS13抑制物或IgG抗体滴度,有效恢复血浆ADAMTS13活性。临床研究证实,iTTP急性发作期使用利妥昔单抗可提升治疗有效率、降低早期死亡率、减少复发率、延长缓解期。利妥昔单抗推荐剂量为每周375 mg/m2,连续应用4周。小剂量利妥昔单抗治疗(每周100 mg,连用4周)效果在探索中。建议利妥昔单抗在血浆置换后开始用药,与下次血浆置换的间隔建议为20~24小时[6,7]。
(4)卡普赛珠单抗(Caplacizumab):卡普赛珠单抗在TTP发病早期使用可以获得最大的益处。通过抑制血小板与血管性血友病因子(VWF)相互作用阻止新的微血栓形成而发挥作用,减少脏器损害。卡普赛珠单抗首次10mg静脉输注,次日起每日10mg皮下注射,停止血浆置换后仍需持续使用30天。
(5)大剂量静脉注射免疫球蛋白:治疗iTPP的效果不及血浆置换,仅适用于难治性TTP患者或多次复发的病例。
(6)其他免疫抑制剂:对利妥昔单抗无效或复发的iTTP患者可选用其他免疫抑制剂,如硼替佐米、环孢素A等。硼替佐米通过阻止ADAMTS13自身抗体产生发挥治疗作用,常用剂量每次1.3mg/m2,皮下注射,每疗程使用四次(d1,d4,d8,d11),1~2疗程。环孢素A常用剂量每日3~5mg/kg体重,并根据血浆环孢素A浓度调整使用剂量。
(7)乙酰半胱氨酸:为还原型谷胱甘肽的前体,可减少多肽链之间的二硫键连接降低VWF多聚化程度,减少组织氧化损伤。在血浆置换后使用有一定的辅助治疗作用。常用剂量每天8g,缓慢静脉输注。
(8)预防性血浆输注:适用于cTTP患者的预防治疗,常用新鲜(冰冻)血浆每次10ml-15ml/kg体重,输注间隔根据患者血小板数变化情况而定,每1~3周一次。反复输注需注意输血相关的疾病传播风险。
(9)重组人ADAMTS13:尤其适合于cTTP患者的预防性治疗,Ⅲ期临床研究结果显示效果显著且安全性良好,患者血小板数保持正常并脱离血浆输注。开展的临床研究正在评估重组人ADAMTS13在iTTP患者治疗中的应用前景。
(10)抗血小板药:iTTP患者病情稳定后可选用潘生丁或/和阿司匹林,对减少复发有一定作用。
(11)支持治疗:本病累及多个器官,需要及时动态评估各器官功能,给予相应的支持治疗,保护器官功能。
3.治疗方案及调整
(1)对临床中度或高度疑似或确诊的TTP(尤其是iTTP)患者应立即开始治疗性血浆置换联合肾上腺皮质激素治疗,并可考虑联合卡普赛珠单抗治疗。根据待测定的ADAMTS13活性及抑制物或IgG抗体结果调整治疗:如测定的患者血浆ADAMTS13活性<10%正常水平且伴抑制物或IgG抗体阳性,符合iTTP,则继续进行上述治疗并及时给予利妥昔单抗治疗;如抑制物阴性,考虑cTTP,可停药激素、并改血浆置换为血浆输注;如患者血浆ADAMTS13活性>20%正常水平,则考虑其他诊断,改用其他相应治疗;当血浆ADAMTS13活性介于10%~20%正常水平之间,需根据临床判断是否继续或停止现行相关治疗。
(2)对复发的iTTP患者,除治疗性血浆置换联合皮质激素治疗外,如之前未用过利妥昔单抗或曾使用利妥昔单抗有效但1年后复发者,加用利妥昔单抗治疗。如用过利妥昔单抗,1年内复发的可选择其他免疫抑制剂(如硼替佐米、环孢素A)清除ADAMTS13抑制物,恢复ADAMTS13活性。
(3)对缓解期iTTP患者应定期进行血常规和ADAMTS13活性监测,警惕疾病复发。本病会对心、脑血管,以及脏器功能和精神状态造成慢性损害,缓解期iTTP患者也应做好相关评估和防治工作。
(4)对缓解期cTTP患者,建议采用血浆输注或密切观察的预防策略,根据患者病情、意愿及可能的不良反应决定治疗选择。对新生儿期发病、有器官损伤的cTTP患者推荐预防治疗。不建议使用血浆源性因子Ⅷ浓缩物,重组ADAMTS13将是更为便捷高效的治疗方法。
(5)iTTP女性妊娠时有较高的疾病复发风险,尤其是持续血浆ADAMTS13活性降低者常常是复发先兆,对母体和胎儿均存在不利影响。预防性治疗可能有助于减少母婴死亡率,如iTTP孕妇血浆ADAMTS13活性<10%可进行血浆置换,每周1~2次;如出现TTP临床表现需每日一次血浆置换;联合使用皮质激素治疗。孕期不建议使用抗CD20单抗。对上述治疗无效,或伴发其他病理产科情况如妊高征等时需提前终止妊娠。对cTTP的孕妇建议自妊娠开始即进行血浆输注,输注间隔随孕期而逐渐缩短,从每2周一次至隔日一次不等;如出现TTP临床表现需增加输注量或改为血浆置换;血浆输注治疗需维持至产后3周。重组ADAMTS13更适合cTTP孕妇的预防治疗。
诊疗流程(图79-1)
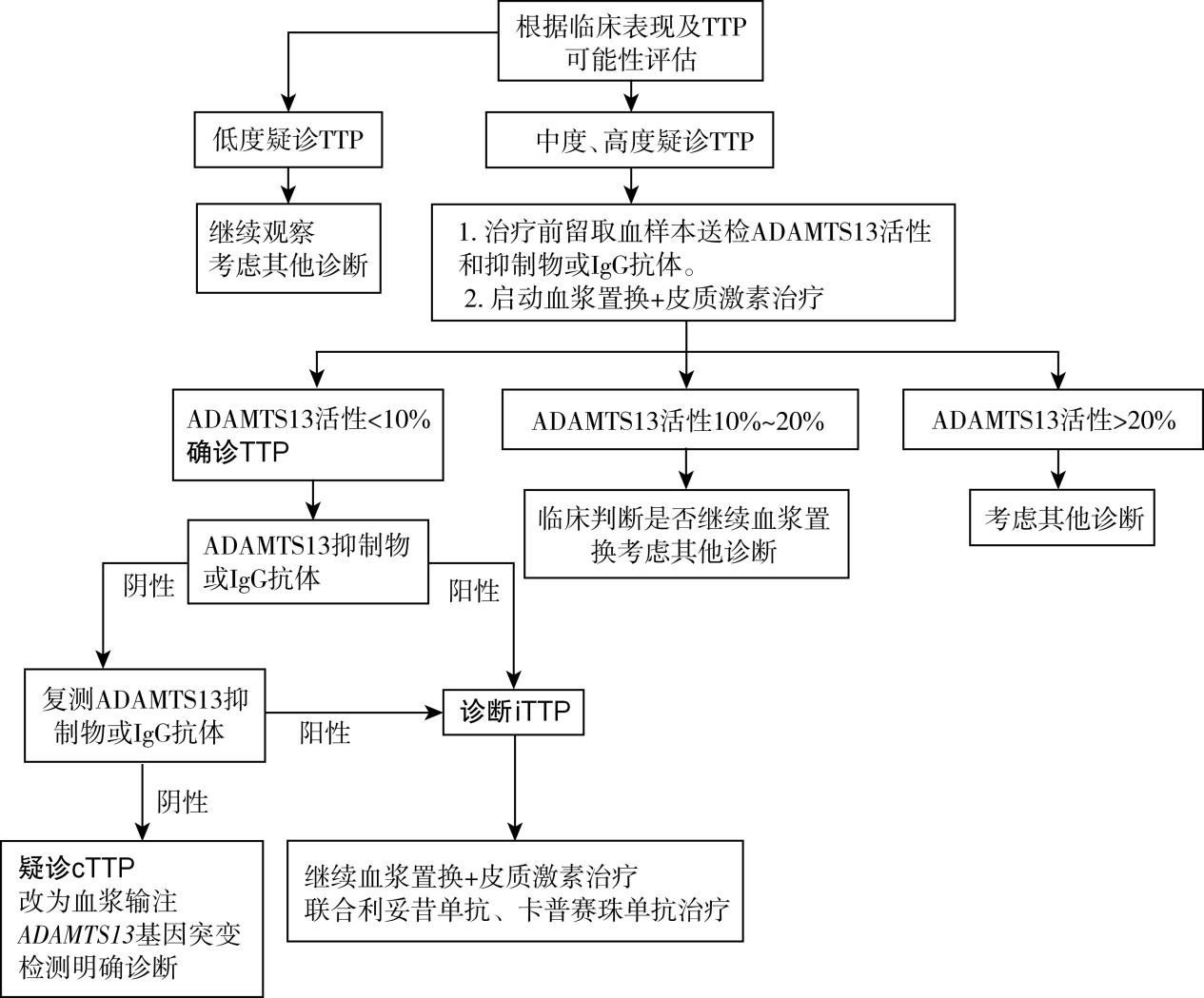
图79-1 TTP的诊疗流程图
参考文献
[1] 中华医学会血液学分会血栓与止血学组.血栓性血小板减少性紫癜诊断与治疗中国指南(2022年版).中华血液学杂志.2022, 43(1): 7-12.
[2] JOLY BS, COPPO P, VEYRADIER A. Thrombotic thrombocytopenic purpura. Blood, 2017,129(21):2836-2846.
[3] BENDAPUDI PK, HURWITZ S, FRY A, et al. Derivation and external validation of the PLASMIC score for rapid assessment of adults with thrombotic microangiopathies: a cohort study. Lancet Haematol, 2017, 4(4):e157-157e164.
[4] CHIASAKUL T, CUKER A. Clinical and laboratory diagnosis of TTP: an integrated approach. Hematology,2018, 2018(1):530-538.
[5] MATSUMOTO M, FUJIMURA Y, WADA H, et al. Diagnostic and treatment guidelines for thrombotic thrombocytopenic purpura (TTP) 2017 in Japan. Int J Hematol, 2017,106(1):3-15.
[6] ZHENG XL, VESELY SK, CATALAND SR, et al. ISTH guidelines for treatment of thrombotic thrombocytopenic purpura. J Thromb Haemost, 2020,18(10):2496–2502.
[7] JESTIN M, BENHAMOU Y, SCHELPE AS, et al. Preemptive rituximab prevents long-term relapses in immune-mediated thrombotic thrombocytopenic purpura. Blood, 2018, 132(20): 2143–2153.
[8] AZOULAY E, BAUER PR, MARIOTTE E, et al. Expert statement on the ICU management of patients with thrombotic thrombocytopenic purpura. Intensive Care Med, 2019,45(11):1518-1539.
[9] DUTT T, SHAW RJ, STUBBS M, et al. Real-world experience with caplacizumab in the management of acute TTP. Blood. 2021,137(13):1731-1740.
[10] LI GW, RAMBALLY S, KAMBOJ J, et al. Treatment of refractory thrombotic thrombocytopenic purpura with N-acetylcysteine: a case report. Transfusion, 2014,54(5):1221-1224.
[11] FERRARI B, PEYVANDI F.How I treat thrombotic thrombocytopenic purpura in pregnancy.Blood, 2020,136(19):2125-2132.


