174、神经母细胞瘤
罕见病诊疗指南(2025年版)
概述 神经母细胞瘤(neuroblastoma,NB)泛指一系列外周神经母细胞性肿瘤(包括:神经母细胞瘤、节细胞性神经母细胞瘤和节细胞神经瘤),这些肿瘤起源于原始交感神经节细胞,是一组临床表现及预后差异很大的疾病,从肿瘤播散、转移、患儿死亡,到肿瘤发展成熟为良性的节细胞神经瘤或自发消退等不同临床转归均可出现。NB 可转移至淋巴结、骨髓、骨骼、硬脑膜、肝脏和皮肤,少数情况下也会转移至肺部和中枢神经系统,临床需要外科、内科、放疗科、移植科以及影像科、病理科、营养科、心理科、疼痛科等多学科联合诊治。
病因及流行病学
NB来源于未分化的交感神经节细胞,故凡有胚胎性交感神经节细胞的部位,都可发生肿瘤。肾上腺是最常见的原发部位,其次是腹部、胸部、颈部和盆腔交感神经节,约1%的病人未能发现原发肿瘤。
NB的发病机制涉及多种分子和细胞遗传学因素,NB表现出的1p、11q缺失、17q获得等染色体数目或结构的改变及基因改变,均与预后较差相关。基因改变包括MYCN扩增,ALK和PHOX2B的种系或体细胞突变,ARTX和TERT位点重排。MYCN扩增、ATRX和TERT突变在高危患者中占主导地位,导致端粒维持,并结合RAS和/或p53途径突变,增加肿瘤侵袭性,预后不良。此外,基因表达的失调,特别是MYCN、ALK、PHOX2B、LIN28B的过表达,通过改变细胞增殖与分化之间的平衡,在NB的发生和发展中发挥关键作用。
NB几乎只发生于儿童,儿童占所有患者的97%,每年发病率约(0.3~5.5)/10万。大多为散发,仅有1%~2%的病例为家族性(即遗传性)。根据国家儿童肿瘤监测中心最新年报,NB的发病率与年龄相关,诊断时的中位年龄为17.3个月,40%的患者在1岁之前即被诊断。
临床表现
根据原发肿瘤和转移瘤灶的部位及范围,临床表现有所不同。局限性肿瘤患者可无症状,肿瘤晚期的儿童在就诊时一般状况差,通常有全身症状。
1.一般症状 不规则发热、乏力、消瘦、纳差、贫血、骨痛、头痛、恶心、呕吐、腹泻等。
2.肿瘤压迫症状 腹部肿瘤可表现为腹痛或腹部胀满感,腹部肿块,甚至肠梗阻、便秘、排尿困难等;胸部肿瘤可表现咳嗽、喘憋、呼吸困难等;颈部和纵隔肿瘤可出现Horner综合征(病灶同侧上睑下垂、瞳孔缩小和无汗症)、一侧上肢疼痛、活动及感觉异常等;椎旁肿瘤经神经孔侵犯椎管,引起硬膜外脊髓压迫从而出现疼痛、运动或感觉障碍、大便失禁和/或尿潴留。
3.肿瘤浸润、转移瘤的症状 NB常见的转移部位为骨髓、骨骼、肝、皮肤和淋巴结。转移至骨可表现肢体疼痛、跛行。肿瘤浸润眶周骨可引起特征性的眶周瘀斑(浣熊眼)、眼球突出。肿瘤扩散至皮肤表现为可触及的无痛性皮下结节,可遍及全身。
4.儿茶酚胺代谢物增高症状 包括发作性多汗、兴奋、心悸、面部潮红、苍白、头痛、高血压及心动过速等。
5.其他原因不能解释的分泌性腹泻 是一种副肿瘤综合征,肿瘤分泌血管活性肠肽(vasoactive intestinal polypeptide, VIP)而表现顽固腹泻。
6.有些病例合并眼阵挛-肌阵挛-共济失调综合征 是一种副肿瘤综合征,发生于1%~3%的NB儿童。表现为快速的舞蹈样眼球运动、累及肢体或躯干的肌阵挛和/或共济失调。
辅助检查
1.肿瘤生物学标记检查包括 ①尿儿茶酚胺及其代谢产物(VMA/HVA):最常见的是VMA增高,少数病例HVA增高,或两者均增高。尿VMA协助诊断NB,并用以检测对治疗的反应;②神经元特异性烯醇化酶(NSE):血清NSE也是NB的重要标志物之一,但并不特异;③其他:血乳酸脱氢酶(LDH)是一种非特异肿瘤标志物,对预后有判断价值。晚期NB患儿常有血清铁蛋白(SF)增高,经治疗达临床缓解时SF可下降至正常。
2.影像学及核医学检查 ①原发肿瘤及转移瘤灶的B超、CT或MR平扫或增强检查,确定肿瘤的位置、周围组织受累程度,以及肿瘤转移的情况;②123I-MIBG扫描:123I-MIBG扫描在骨骼评估方面优于锝扫描,其检测转移性病灶的灵敏度和特异度更高(有条件的单位可行123I-MIBG检查);③对于MIBG检查阴性患儿可进行18F-FDG PET/CT(fluorine-18-fluoro-2-deoxy-D-glucose positron emission tomography/computed tomography)检查。由于国内开展123I-MIBG核素扫描检查项目的医院十分有限,故建议国内无法接受此检查的神经母细胞瘤患儿可以进行18F-FDG PET/CT检查。
3.病理组织学检查 肿块切除、穿刺活检或切开活检以进行病理检查。
4.骨髓检查 ①骨髓细胞形态学:骨髓穿刺可见瘤细胞集结成团,形似菊花环。但如瘤细胞少而分散,则不易辨认。检测时建议选择2个不同的位置穿刺,以最大限度获得骨髓是否受累依据;②骨髓活检:一般在髂后上棘进行,以进一步明确骨髓是否受累。
5.肿瘤组织或肿瘤检测阳性的骨髓须进行遗传学检查 包括:①染色体数量和质量异常,包括1p、3p、4p或11q缺失;1q、2p或17q获得等;②MYCN基因检测;③肿瘤组织DNA倍数:新鲜肿瘤组织标本通过流式细胞学技术进行检测。
诊断
1.NB诊断标准 确诊NB需满足以下条件之一:①通过光镜对肿瘤组织进行明确的病理诊断;②骨髓涂片或穿刺活检明确含有特征性NB肿瘤细胞(如:巢状或菊花团样排列,免疫细胞学阳性),并伴有尿液或血清儿茶酚胺或代谢物增加。
2.影像学定义的危险因素(image-defined risk factors,IDRFs) IDRFs是通过影像学检查定义的手术危险因素,IDRFs高提示肿瘤全切除有风险或困难,并增加手术并发症的风险(表53-1)。
表53-1 影像学定义的危险因素
影像学定义的危险因素(IDRFs) |
单侧肿瘤延伸到两个体腔,如颈部到胸腔、胸腔到腹腔、腹腔到盆腔 |
颈部 肿瘤包绕颈动脉和/或椎动脉和/或颈内静脉 肿瘤延伸至颅底 肿瘤压迫气管 |
颈胸连接处 肿瘤包绕臂丛神经根 肿瘤包绕锁骨下血管和/或椎动脉和/或颈动脉 肿瘤压迫气管 |
胸部 肿瘤包绕主动脉和/或主动脉分支 肿瘤压迫气管和/或主支气管 下纵隔肿瘤,侵犯T9和T12肋椎连接处 |
胸腹连接处 肿瘤包绕主动脉和/或腔静脉 |
腹腔和盆腔 肿瘤侵犯肝门和/或肝十二指肠韧带 肿瘤包绕肠系膜上动脉在肠系膜根部的分支 肿瘤包绕腹腔干和/或肠系膜上动脉起始部 肿瘤侵犯一侧或双侧肾蒂 肿瘤包绕腹主动脉和/或下腔静脉、髂血管 盆腔肿瘤越过坐骨切迹 |
椎管内肿瘤延伸 水平位超过1/3椎管被侵犯和/或环脊髓软脑膜间隙不可见和/或脊髓信号异常 |
邻近器官/组织受累 包括心包、膈肌、肾脏、肝、十二指肠-胰腺阻塞、肠系膜和其他内脏受侵犯 |
需要记录的情况,但不视为IDRFs 多灶性原发性肿瘤 胸腔积液,伴或不伴恶性细胞 腹水,伴或不伴恶性细胞 |
3.国际神经母细胞瘤危险度分期系统(International Neuroblastoma Risk Group Staging System,INRGSS) INRGSS是术前分期系统,此分期纳入了治疗前IDRFs而非手术切除时的发现,疾病的程度取决于在诊断时(治疗前或手术前)是否有IDRFs和/或转移性肿瘤。INRGSS分为:
L1期——没有涉及重要结构IDRFs的局限性肿瘤;
L2期——有一个或多个IDRFs的局限性肿瘤;
M期——有远处转移病灶(除MS外);
MS期——年龄小于18个月,转移性病灶局限于皮肤、肝脏、和/或骨髓(骨髓肿瘤细胞在10%以下;MIBG扫描骨和骨髓显像阴性;原发肿瘤可以是L1或L2)
1.国际神经母细胞瘤危险度分组(internationalneuroblastoma risk group,INRG)(表53-2)
表53-2 国际神经母细胞瘤危险度分组
INRGSS | 诊断年龄/月 | 组织学类型 | 肿瘤分化程度 | MYCN | 11q畸变 | 倍性 | 危险度 |
L1/L2 |
| 节细胞神经瘤 节细胞性神经母细胞瘤-混杂型 |
|
|
|
| 极低危 |
L1 |
| 除节细胞神经瘤或节细胞性神经母细胞瘤-混杂型之外 |
| 不扩增 |
|
| 极低危 |
扩增 |
|
| 高危 | ||||
L2 | <18 | 除节细胞神经瘤或节细胞性神经母细胞瘤-混杂型之外 |
| 不扩增 | 无 |
| 低危 |
有 |
| 中危 | |||||
≥18 | 节细胞性神经母细胞瘤-结节型 神经母细胞瘤 | 分化型 | 不扩增 | 无 |
| 低危 | |
有 |
| 中危 | |||||
分化差或未分化型 | 不扩增 |
| |||||
| 扩增 |
|
| 高危 | |||
M
| <18 |
|
| 不扩增 |
| 超二倍体 | 低危 |
<18 |
|
| 不扩增 |
| 二倍体 | 中危 | |
<18 |
|
| 扩增 |
|
| 高危 | |
≥18 |
|
|
|
|
| 高危 | |
MS
| <18 |
|
| 不扩增 | 无 |
| 极低危 |
有 |
| 高危 | |||||
扩增 |
|
| 高危 |
鉴别诊断
1.嗜铬细胞瘤 嗜铬细胞瘤是起源于肾上腺髓质的肿瘤,通常分泌儿茶酚胺,患者可表现为高血压、心动过速症状,尿中儿茶酚胺及其代谢物增加,MIBG摄取阳性,需要和NB鉴别。嗜铬细胞瘤在儿童中罕见,常常和家族性疾病相关,60%~90%出现持续性高血压,典型三联征包括发作性头痛、发汗和心动过速,其他少见症状体征包括惊恐发作、直立性低血压、苍白、便秘、视物模糊、视盘水肿、体重减轻、多尿、烦渴、注意缺陷多动障碍等。嗜铬细胞瘤多数为良性,肿瘤通常有完整包膜,与周围正常组织分界清楚,很少发生转移,通过手术完整切除即可治愈,但有10%嗜铬细胞瘤是恶性。通过临床表现、体征、病理可与NB鉴别。
2.肾上腺皮质肿瘤 肾上腺皮质腺瘤是发生于肾上腺皮质的良性肿瘤,肾上腺皮质癌是发生于肾上腺皮质的恶性肿瘤。其在影像上表现为肾上腺占位,需要和原发于肾上腺的NB鉴别。分泌激素的功能性肾上腺皮质肿瘤,可表现出雄激素和/或皮质醇产生增加(皮质醇过多或库欣综合征)的体征和症状,如男性化综合征,少部分表现为雌激素或醛固酮过多。多数肾上腺皮质腺瘤的直径小于4cm,而肾上腺皮质癌多直径>4cm。肾上腺皮质分泌性肿瘤,可通过临床表现、激素水平,与NB相鉴别;对于无分泌功能的肿瘤,则需要组织病理进行鉴别诊断。
3.肾脏肿瘤 发生于肾脏的肿瘤,如肾母细胞瘤、肾脏恶性横纹肌样瘤、肾透明细胞肉瘤等,均可表现为腹部包块、肾脏及肾上腺区巨大占位,需要与NB相鉴别。肾母细胞瘤在CT影像上常见坏死囊变区和新旧同时存在的出血灶,钙化少见,肿块较大时跨过中线、腹膜后大血管被推移但不包绕,可见肾静脉和下腔静脉内瘤栓,肺转移比较常见。肾透明细胞肉瘤常伴有骨转移。NB瘤灶呈浸润性生长,包绕腹膜后大血管,70%~80%可见多发钙化灶,肺转移少见,而骨髓及骨骼转移常见。在临床表现及影像鉴别有困难时,需要组织病理确诊。
4.小圆细胞恶性肿瘤 NB组织病理在光学显微镜下呈现为小的圆形蓝色细胞的聚集,需要与其他小细胞恶性肿瘤相鉴别,如尤文肉瘤、横纹肌肉瘤、小细胞骨肉瘤、淋巴母细胞淋巴瘤、滑膜肉瘤、间叶性软骨肉瘤等,需进一步行免疫组织化学染色,必要时行基因检测区别。
5.急性白血病 NB发生骨髓转移时,可表现为发热、乏力、腿痛,血常规出现贫血、血小板减少,骨髓中出现肿瘤细胞,需要和儿童常见的血液系统肿瘤,如急性白血病等相鉴别。通过影像学查找原发瘤灶,骨髓中可见特征性菊花团样肿瘤细胞,尿液或血清儿茶酚胺或代谢物增加,以此进行两者的鉴别。
6.全身性疾病 以发热、骨痛、全身症状为表现者,需与感染性疾病、风湿热、骨髓炎、类风湿等全身性疾病相鉴别。完善影像学检查,必要时行全身PET/CT寻找原发瘤灶,并完善尿液或血清儿茶酚胺或代谢物检测。必要时需要行病理活检明确诊断。
治疗
1.极低危、低危NB治疗 对于极低危、低危NB,以手术切除为主。有症状、肿瘤未全切、术后进展、预后不良病理类型、不良分子生物学特征等病例,可给予化疗,化疗药物包括卡铂、环磷酰胺、阿霉素和依托泊苷等,一般4个疗程。
2.中危NB的治疗 病初未行肿瘤切除的患者,术前化疗2~4疗程,可行手术切除,术后根据残留病灶、病理、分子生物学等情况酌情给予2~4疗程化疗,总疗程6~8个。化疗药物包括卡铂、环磷酰胺、阿霉素和依托泊苷等。
3.高危NB的治疗 高危NB的治疗,包括三个阶段,即诱导治疗阶段(强化疗和手术)、巩固治疗阶段(造血干细胞移植和放射治疗)、维持治疗阶段(GD2单克隆抗体免疫治疗和13-顺式维A酸治疗)。
(1)诱导化疗:明确高危NB诊断后,接受诱导化疗,每2个疗程进行疗效评估,诱导化疗总疗程6~8个。国内国际各研究机构的诱导化疗方案有所不同,可参考选择。国家卫生健康委员会神经母细胞瘤诊疗规范(2019版)应用长春新碱+环磷酰胺+阿霉素、顺铂+依托泊苷交替方案诱导化疗7疗程。中国抗癌协会CCCG-NB-2021专家共识及美国儿童肿瘤协作组(Children’s Oncology Group, COG)应用环磷酰胺+托泊替康、顺铂+依托泊苷、环磷酰胺+阿霉素+长春新碱交替方案诱导化疗6疗程。国际儿童肿瘤协会欧洲神经母细胞瘤协作组(International Society of Pediatric Oncology European Neuroblastoma Group,SIOPEN)应用快速COJEC方案8周期诱导化疗,包括长春新碱+卡铂+依托泊苷、长春新碱+顺铂、长春新碱+依托泊苷+环磷酰胺交替,若转移灶对8疗程快速COJEC治疗反应不充分,可增加2疗程托泊替康+长春新碱+阿霉素。德国儿童血液肿瘤协作组(German Pediatric Oncology and Hematology Group,GPOH)应用顺铂+依托泊苷+长春地辛、长春新碱+达卡巴嗪+异环磷酰胺+阿霉素交替方案诱导化疗6疗程。
(2)手术:完全切除原发瘤灶及区域内转移淋巴结是最好的治疗方法,如果手术并发症不可接受,则行部分切除,残留病灶通过放化疗继续治疗。病初没有全身转移或无IDRFs的高危NB病例,可在病初先行原发瘤灶的切除;病初未行手术切除的高危患者,可于化疗3~4疗程后,待原发瘤灶缩小,肿瘤标记物下降,骨髓转阴,转移灶局限的情况下,行手术切除原发瘤灶。通过化疗使转移瘤灶局限后,可行手术切除转移灶,如肝或肺孤立病灶。持续存在的颈部转移灶可行颈部淋巴结清扫术。
(3)造血干细胞移植:高危组NB患者的巩固治疗阶段包括清髓化疗及自体造血干细胞移植,以进一步清除体内微小残留病灶。几项大型随机对照研究结果显示,与传统化疗(22%~31%)相比,自体造血干细胞移植治疗的3年无事件生存率(EFS)(34%~47%)明显提高。准备行移植的患者,可于完成手术及6~7疗程的诱导期强化疗后行自体造血干细胞移植。单次移植预处理方案可选择白消安 + 美法仑,或选择卡铂+依托泊苷 + 美法仑。串联自体造血干细胞移植可进一步加强巩固治疗,清除体内微小残留病灶,降低肿瘤负荷。串联移植的第一次预处理方案可选择塞替哌+环磷酰胺,第二次预处理方案为减量的卡铂+依托泊苷+美法仑。美国COG的一项随机临床研究显示,在诱导治疗后采用串联自体干细胞移植对比单次移植,可改善高危NB患者的无事件生存率,3年EFS率为62% vs.48%(P=0.006),而3年OS率74% vs. 69%(P=0.25);移植后患者继续给予GD2单克隆抗体免疫治疗,串联移植较单次移植,3年EFS和OS均有改善(EFS: 73.3% vs.54.7%,P=0.004; OS: 84.0% vs.73.5%,P=0.04)。
(4)放射治疗:所有高危NB均需在造血干细胞移植后,接受原发瘤灶、持续存在的转移灶的放疗,以提高局部控制率。对原发瘤灶,推荐放疗剂量21.6Gy;对持续存在的转移灶,局部可推量至30~36Gy剂量。
(5)GD2单克隆抗体:高危NB巩固阶段后的维持治疗包括抗GD2单克隆抗体免疫治疗和13-顺式维A酸口服治疗,进一步清除体内微小残留病灶。GD2在NB细胞表面100%特异性表达,因此GD2单克隆抗体是针对GD2的免疫靶向药物。根据属源不同,抗GD2抗体分为鼠源、嵌合型和人源。目前,国际上已获批上市用于临床治疗的GD2单克隆抗体分别是Ch14.18、Ch14.18/CHO和Hu3F8。
其中,Ch14.18/CHO于2021年在中国获批进入临床应用,适用于治疗①≥12月龄的高危NB患者,这些患者既往接受过诱导化疗且至少获得部分缓解,并且随后进行过清髓性治疗和干细胞移植治疗;也适用于治疗②伴有或不伴有残留病灶的复发或难治性NB。在治疗复发性NB患者之前,应采取适当措施使活动性进展疾病保持稳定。SIOPEN研究显示,Ch14.18/CHO用于清髓化疗及干细胞移植后的初治高危NB维持治疗,对比未接受免疫治疗患者,可使高危NB患者生存获益。国内推荐Ch14.18/CHO联合13-顺式维A酸±粒细胞巨噬细胞集落刺激因子(GM-CSF)用于初治高危NB维持治疗,共5个疗程,每个疗程35天。
(6)13-顺式维A酸治疗:13-顺式维A酸又名异维甲酸或异维A酸,是一种强分化诱导剂,具有控制细胞分化、增殖和凋亡的能力,它可以诱导NB分化,达到治疗肿瘤作用。13-顺式维A酸用于高危NB的维持治疗阶段。剂量160mg/(m2·d)[<12kg,5.33mg/(kg·d)],每天2次口服,每月服用2周,口服6个月。13-顺式维A酸是维生素A的衍生物,服用期间会出现维生素A过多综合征样反应,应用过程中注意避免同时服用其他含有维生素A的药物或营养补充剂。
4.复发/难治高危NB的治疗 尽管随着多种治疗手段进步、多学科协作诊疗模式的成熟开展,高危NB的生存有所提高,但仍有近一半的患者出现复发或对前期治疗无反应。复发/难治高危患者的生存率很低,4年无进展生存率6%,总生存率20%,中位无进展生存期为6.4个月。目前国内外对于复发/难治NB尚无统一、确切有效的治疗方案。
(1)化疗:复发或难治性NB对化疗反应低,预后不佳。针对复发部位,原发灶或转移灶、骨髓,可选择的化疗方案包括:伊立替康+替莫唑胺、托泊替康+环磷酰胺、卡铂+伊立替康+替莫唑胺、异环磷酰胺+卡铂+依托泊苷、卡铂+伊立替康+依托泊苷等。
(2)GD2单克隆抗体:Hu3F8是人源化GD2单克隆抗体,于2022年在中国获批进入临床应用,适用于治疗对既往治疗表现出部分缓解、轻微缓解或疾病稳定的复发性或难治性骨或骨髓高危NB的1岁及以上患者。Hu3F8联合GM-CSF治疗高危NB,尤其是伴有骨/骨髓残留病灶的难治/复发性高危NB患者,有明显生存获益。Hu3F8联合伊立替康+替莫唑胺,Ch14.18/CHO单药或联合伊立替康+替莫唑胺治疗复发/难治性高危NB,均显示了较好客观缓解率。
(3)ALK抑制剂:ALK基因的遗传改变是高危NB预后差的独立预测因子,ALK突变/扩增常常与高危NB的MYCN扩增同时发生,存在ALK突变/扩增的高危NB的5年OS为28%,无ALK改变者为51%,尤其是在转移性病例。美国费城儿童医院应用三代ALK抑制剂联合化疗托泊替康+环磷酰胺治疗ALK-驱动的难治/复发高危NB的Ⅰ期临床试验显示出一定疗效,25%患者达到了最佳疗效(完全缓解+部分缓解),62%患者有效(完全缓解+部分缓解+轻微缓解)。
(4)造血干细胞移植:自体干细胞移植,其本质是清髓化疗加自体干细胞解救,可作为难治/复发高危NB的治疗选择。但复发再化疗后,干细胞的采集在一定程度上受限,如果自身干细胞数量满足移植要求,可以选择。异基因造血干细胞移植,移植后重建的供体免疫系统产生的移植物抗肿瘤效应,可达到清除MRD和预防疾病复发目的,是复发/难治NB患者的一种治疗选择,可单独使用,或者移植后联合GD2单克隆抗体免疫治疗。但造血干细胞移植对于难治/复发NB疗效尚缺乏大规模临床数据结果。
(5)放射性核素治疗:NB肿瘤细胞在其细胞膜上表达去甲肾上腺素(NE)转运蛋白,并通过NE转运蛋白吸收MIBG,碘-131(131I)-MIBG可用于NB治疗。131I-MIBG可单独应用,或联合化疗、联合干细胞移植用于复发/难治NB的治疗,均显示了一定疗效。
(6)嵌合抗原受体T细胞治疗:嵌合抗原受体T细胞(chimeric antigen receptor-engineered T cells,CAR-T)能特异性识别、结合并杀伤具有特异性表面标志的肿瘤细胞,是治疗难治/复发NB的研究热点。目前针对NB的GD2、L1-CAM、GPC2、B7-H3等靶点的CAR-T治疗,均有开展的临床前/临床研究。尤其是GD2-CART治疗难治/复发NB,1/2期临床试验结果显示了一定有效性,安全性可控,但尚缺乏大规模的研究数据。
疗效评估
2017年修订后的国际神经母细胞瘤评估标准(International Neuroblastoma Response Criteria,INRC)评估包括原发瘤灶、转移的软组织和骨以及骨髓的反应(表53-3~6)。其中原发瘤灶、转移的软组织,使用RECIST标准并结合123I-MIBG或18F-FDG-PET-CT(如果肿瘤组织MIBG无摄取)进行评估。MIBG或PET-CT替代99mTc骨扫描评估骨转移,骨髓通过组织学或细胞学进行评估,尿儿茶酚胺水平不包括在反应评估中。
表53-3 原发瘤灶评估反应
评估反应 | 影像评估 |
CR | 原发灶残留<10mm,且原发部位在MIBG或PET-CT无摄取 |
PR | 原发灶最长径减少≥30%,且原发部位MIBG或PET-CT摄取提示稳定、改善或消失 |
PD | 原发灶最长径增加>20%,且最长径绝对值至少增加5 mm |
SD | 原发灶既没有达到PR缩小,也没有达到PD增加 |
表53-4 软组织转移灶评估反应
评估反应 | 影像评估 |
CR | 转移灶消失:非原发的转移性靶病灶或非靶病灶<10 mm,且靶病灶淋巴结短径<10 mm,且非原发病灶的MIBG或FDG-PET无摄取 |
PR | 非原发靶病灶的直径总和缩小≥30%,且符合以下:非靶病灶稳定或缩小、无新发病灶、MIBG绝对骨评分降低≥50%(相关骨评分0.1~0.5),或FDG-PET骨病变数量减少≥50% |
PD | 任何一项:①CT/MRI显示新的软组织病变,且MIBG或FDG-PET摄取;②影像发现新的软组织病变,病理确认为神经母细胞瘤或节细胞性神经母细胞瘤;③MIBG显示新发骨摄取病灶;④FDG-PET显示新发骨摄取病灶,且CT/MRI一致提示,或病理证实为神经母细胞瘤或节细胞性神经母细胞瘤;⑤非原发软组织靶病灶最长径增加≥20%,且直径之和至少增加5mm;⑥相对MIBG评分≥1.2 |
SD | 非原发灶病灶既没有达到PR缩小,也没有达到PD增加 |
表53-5 骨髓转移灶评估反应
评估反应 | 细胞学/组织学 |
CR | 无肿瘤细胞浸润 |
PD | 无骨髓转移病人,再评估时出现骨髓>5%肿瘤浸润;或有骨髓转移病人,再评估时骨髓肿瘤浸润较前增加>2倍,且肿瘤浸润>20% |
MD | 骨髓≤5%的肿瘤浸润,再评估时肿瘤浸润0~5%;或骨髓无转移病人,再评估时骨髓≤5%肿瘤浸润;或骨髓>20%肿瘤浸润,再评估时肿瘤浸润0~5% |
SD | 骨髓有肿瘤浸润,再评估时骨髓肿瘤仍浸润>5%,但不符合CR、MD或PD标准 |
表53-6 总体评估反应
评估反应 | 评估标准 |
CR | 所有评估项目均符合CR |
PR | 至少一部分评估为PR,其他为CR、MD(骨髓)、PR(软组织或骨)或未受累,无PD |
MR | 至少一部分评估为PR或CR,至少其他一部分为SD,无PD |
SD | 一部分评估为SD,其他部分评估不优于SD或者未受累,无PD |
PD | 任何有出现PD的部分 |
注:CR(complete response, 完全反应),PR(partial response,部分反应),MR(minor response,轻微反应),SD(stable disease,疾病稳定),PD(progressive disease,疾病进展),MD(minimal disease,微小疾病)。
诊疗流程 (图53-1)
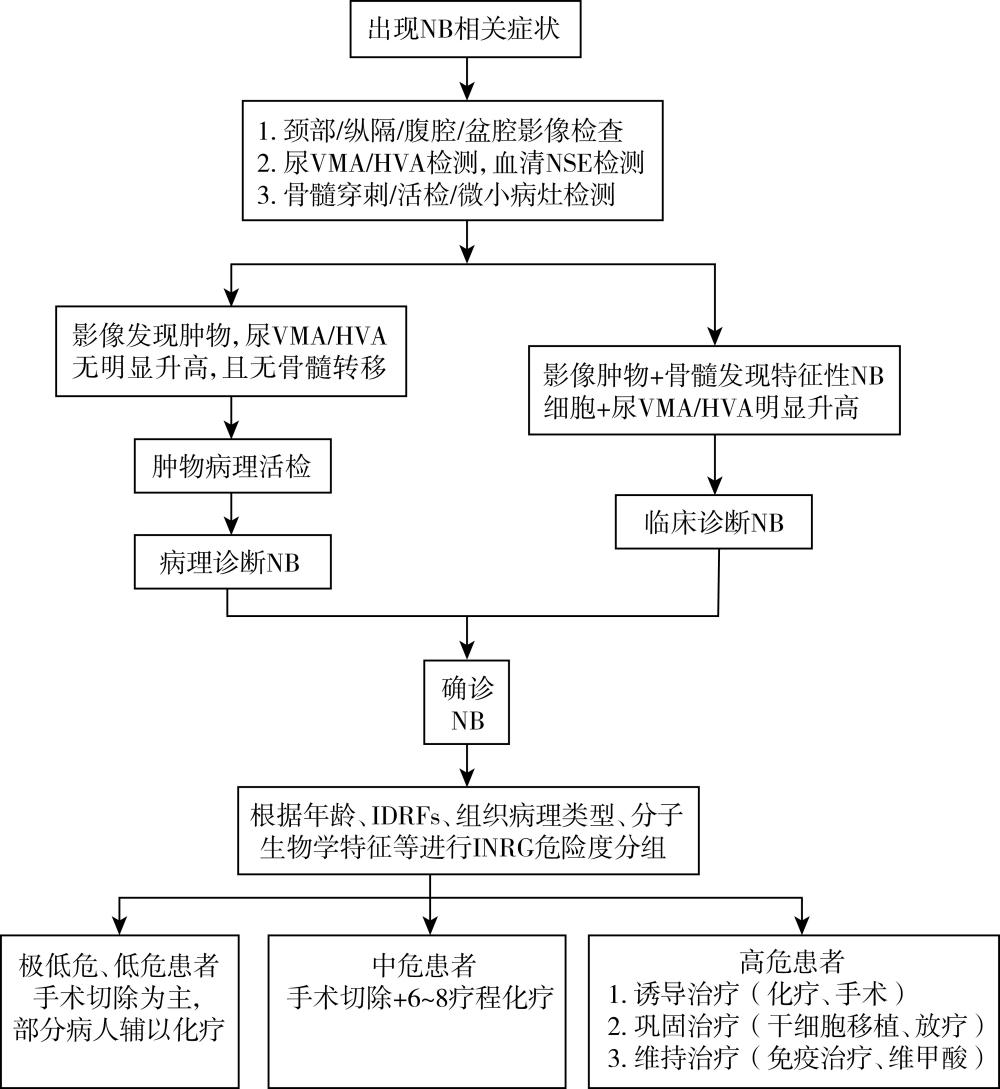
图53-1 神经母细胞瘤诊疗流程
参考文献
[1] Brodeur GM, Pritchard J, Berthold F, et al. Revisions of the international criteria for neuroblastoma diagnosis, staging, and response to treatment. J Clin Oncol, 1993, 11(8): 1466-1477.
[2] Monclair T, Brodeur GM, Ambros PF, et al.The International Neuroblastoma Risk Group (INRG) staging system: an INRG Task Force report. J Clin Oncol,2009, 27(2):298-303.
[3] Cohn SL, Pearson ADJ, London WB,et al. The International Neuroblastoma Risk Group (INRG) classification system: an INRG Task Force report. J Clin Oncol,2009,27(2):289-297.
[4]国家卫生健康委员会.儿童神经母细胞瘤诊疗规范(2019年版).[2024-09-01]. http://www.nhc.gov.cn/yzygj/s3593/201909/5f1d3329606e4cd2aa6e501603703ee4/files/eaee74feeca94706b1fbc2ac85297762.pdf.
[5]中国抗癌协会小儿肿瘤专委会.儿童神经母细胞瘤诊疗专家共识CCCG-NB-2021方案.中华小儿外科杂志,2022,43(7):588-598.
[6] Qiu B, Matthay KK. Advancing therapy for neuroblastoma. Nat Rev Clin Oncol, 2022 ,19(8):515-533.
[7] Simon T, Hero B, Schulte JH, et al. 2017 GPOH guidelines for diagnosis and treatment of patients with neuroblastic tumors. Klin Padiatr, 2017,229(3):147-167.
[8] Matthay KK, Reynolds CP, Seeger RC, et al. Long-term results for children with high-risk neuroblastoma treated on a randomized trial of myeloablative therapy followed by 13-cis-retinoic acid: a children's oncology group study. J Clin Oncol, 2009,27(7):1007-13.
[9] Berthold F, Boos J, Burdach S,et al. Myeloablative megatherapy with autologous stem-cell rescue versus oral maintenance chemotherapy as consolidation treatment in patients with high-risk neuroblastoma: a randomised controlled trial. Lancet Oncol,2005,6(9):649-58.
[10] Ladenstein R, Pötschger U, Pearson ADJ, et al. Busulfan and melphalan versus carboplatin, etoposide, and melphalan as high-dose chemotherapy for high-risk neuroblastoma (HR-NBL1/SIOPEN): an international, randomised, multi-arm, open-label, phase 3 trial. Lancet Oncol,2017,18(4):500-514.
[11] Granger MM, Naranjo A, Bagatell R, et al. Myeloablative busulfan/melphalan consolidation following induction chemotherapy for patients with newly diagnosed high-risk neuroblastoma: children's oncology group trial ANBL12P1. Transplant Cell Ther,2021,27(6):490.e1-490.e8.
[12] Park JR, Kreissman SG, London WB, et al. Effect of tandem autologous stem cell transplant vs single transplant on event-free survival in patients with high-risk neuroblastoma: a randomized clinical trial. JAMA,2019,322(8):746-755.
[13] Ladenstein R, Pötschger U, Valteau-Couanet D, et al.Investigation of the role of dinutuximab beta-based immunotherapy in the SIOPEN High-Risk Neuroblastoma 1 Trial (HR-NBL1). Cancers (Basel),2020,12(2):309.
[14] GD2抗体达妥昔单抗 β 治疗神经母细胞瘤的临床应用专家共识(2021年版).临床儿科杂志,2022,40(1):14-20.
[15] London WB, Bagatell R, Weigel BJ, et al. Historical time to disease progression and progression-free survival in patients with recurrent/refractory neuroblastoma treated in the modern era on Children's Oncology Group early-phase trials. Cancer, 2017,123:4914-4923.
[16] Kushner BH, Cheung IY, Modak S,et al. Humanized 3F8 anti-GD2 monoclonal antibody dosing with granulocyte-macrophage colony-stimulating factor in patients with resistant neuroblastoma: a phase 1 clinical trial. JAMA Oncol, 2018,4(12):1729-1735.
[17] Mora J, Kushner BH, Flores MA, et al. Naxitamab-based chemoimmunotherapy for resistant high-risk neuroblastoma: preliminary results of HITS pilot/phaseⅡstudy. J Clin Oncol, 2019,37(15_suppl):10025.
[18] Wieczorek A, Zaniewska-Tekieli A, Ehlert K, et al. Dinutuximab beta combined with chemotherapy in patients with relapsed or refractory neuroblastoma. Front Oncol,2023, 13:1082771.
[19] Goldsmith KC, Park JR, Kayser K, et al. Lorlatinib with or without chemotherapy in ALK-driven refractory/relapsed neuroblastoma: phase 1 trial results. Nat Med,2023, 29(5):1092-1102.
[20] Park JR, Bagatell R, Cohn SL, et al. Revisions to the international neuroblastoma response criteria: a consensus statement from the national cancer institute clinical trials planning meeting. J Clin Oncol, 2017, 35(22): 2580-2587.


