161、化脓性汗腺炎
罕见病诊疗指南(2025年版)
概述 化脓性汗腺炎(hidradenitis suppurativa,HS)又称反常性痤疮(acne inversa,AI),是一种因毛囊闭锁导致毛囊皮脂腺单位受累的慢性复发性炎症性皮肤病,好发于腋下、腹股沟、会阴、肛周等顶泌汗腺分布区域,主要表现为青春期开始出现的疼痛性、深在的炎症性结节,继而形成脓肿、窦道和瘢痕形成,部分病人合并多种皮肤或系统性并发症,严重影响患者的生活质量。HS/AI发病与遗传、炎症与免疫等多种因素相关。本病治疗困难,目前的治疗目的仍然是以控制皮损发作频率、严重程度以及发作持续时间、提高患者生活质量为主。医生应根据病情严重程度分级治疗,药物治疗包括抗生素、维A酸类、生物制剂、免疫抑制剂以及抗雄激素药物等,辅助治疗包括外科手术或光电治疗。
病因和流行病学
基于不同的人群统计的HS/AI患病率报告差异较大,欧美人群报告患病率为0.05%~4.1%,男女比例约为1∶3,其中30%~40%患者有家族史;亚洲人群的患病率为0.04%~0.06%,男女比例为(1.6~2.5)∶1,一项基于中国人皮肤科门诊就诊者的HS患病率调查报告患病率为0.03%,且男性多于女性。
HS/AI的病因与发病机制尚未完全明确,相关因素包括遗传、免疫与炎症、微生物感染、肥胖及吸烟等。这些因素可能参与毛囊口表皮细胞角化过度,造成毛囊口闭塞,毛囊内容物潴留,导致毛囊扩张、破裂以及继发炎症反应,病情反复发作引起组织结构破坏。在遗传方面,已经明确γ-分泌酶(γ-secretase)是家族性HS的致病基因。γ-分泌酶复合物是由早老素(presenilin,PS1)、早老素增强子-2(presenilin enhancer-2,PEN-2)、呆蛋白(nicastrin,NCSTN)和前咽缺陷蛋白-1(anterior-pharynx- defective-1,APH1)四个亚基组成的异四聚体蛋白复合物,其中发现早老素1、早老素增强子2和呆蛋白基因突变是家族性HS/AI患者的遗传因素。γ分泌酶参与固有免疫及毛囊上皮细胞增生与分化,其功能丧失性突变可能通过影响Notch等信号通路参与HS/AI发病。此外,γ分泌酶的功能失活可导致表皮生长因子受体功能异常,引起表皮角质形成细胞过度增殖,使毛囊口角化异常,从而参与HS/AI发病。在散发的HS/AI患者中并未发现γ分泌酶基因突变,而家族性与散发性HS/AI的病理与临床改变并未发现存在不同。
在免疫与炎症方面,毛囊上部阻塞、毛囊周围炎症细胞浸润、毛囊皮脂腺单位的固有免疫反应异常在HS/AI发病中起重要作用。HS/AI患者皮损处肿瘤坏死因子(tumor necrosis factor,TNF)-α、白细胞介素(interleukin,IL)-17及与活化的胱天蛋白酶1相关的IL-1β与IL-18水平均明显升高,且存在干扰素(interferon,IFN)-γ、IL-12、IL-23、IL-32等 型辅助性T细胞(Th1)、Th17相关的细胞因子聚集,而皮损中IL-13等Th2相关的细胞因子水平与Th1、Th17相关的细胞因子水平呈负相关。体外培养从患者毛囊中分离出的角质形成细胞和外周血单个核细胞受到刺激后,分泌趋化因子(如CCL5、CCL20和CCL27)和细胞因子(如TNF-α、IL-1β、IL-6)的水平异常升高,而具有免疫调节活性的CXCL16不足,均提示异常的固有免疫应答在HS/AI炎症过程中发挥作用。此外,也有研究显示,HS/AI患者血液中补体C5a和C5b-9的浓度显著升高,刺激外周血单个核细胞产生过量TNF-α等。
在微生物方面,HS/AI患者皮损处菌群主要组成为棒状杆菌、卟啉单胞菌和嗜胨菌属,而痤疮丙酸杆菌比健康人显著减少;非皮损处菌群分类变化不显著 ,微生物可能参与了继发感染及相关的炎症反应。67%的慢性病灶及75%的病灶周围皮肤中可检出生物膜,该结构具有抵抗宿主免疫防御和抗生素的能力,可能导致诱发病情急性加重。此外,肥胖与吸烟是HS/AI的相关危险因素,皱褶处皮肤机械摩擦,汗液潴留增加或炎症细胞因子分泌增加可能影响HS/AI肥胖患者的病情变化。香烟中的尼古丁及苯并芘可能与表皮增生、毛囊角栓以及炎症反应有关。
临床表现
HS/AI的典型皮损表现为成对出现的黑头粉刺、炎症性丘疹、结节、囊肿、脓肿、窦道和瘘管,后期可出现皮肤挛缩及瘢痕形成,部分患者还可合并藏毛窦。皮损反复发作,引起患者疼痛或明显触痛。本病可伴随或继发多种系统性疾病及表现,如糖尿病、淋巴水肿、贫血、低蛋白血症、自身炎症性疾病[尤其是炎症性肠病、炎症性关节病、滑膜炎-痤疮-脓疱病-骨肥厚-骨炎(synovitis-acne-pustulosis-hyperostosis-osteitis,SAPHO)综合征、坏疽性脓皮病-痤疮-化脓性汗腺炎综合征(PASH综合征)、化脓性关节炎-坏疽性脓皮病-痤疮综合征(PAPA综合征);化脓性关节炎-坏疽性脓皮病-痤疮-化脓性汗腺炎综合征(PAPASH综合征)等],患者发生抑郁与焦虑等不少见,长期慢性溃疡性皮损可继发鳞状细胞癌等。根据临床表型不同,HS/AI可分为寻常型、摩擦疖肿型、瘢痕毛囊炎型、聚合型、综合征型及异位型,各型特征见表40-1。HS合并聚合性痤疮、头部脓肿性穿掘性毛囊炎及毛囊周围炎时称为毛囊闭锁三联征,如同时伴有藏毛窦则被称为毛囊闭锁四联症。

辅助检查
HS的诊断通常无需皮肤活检及影像学检查。但当诊断不明时,活检有助于排除其他疾病。HS的组织病理学表现因病变阶段而异。早期常见特征包括毛囊口角化过度、毛囊堵塞、毛囊扩张和淋巴细胞性毛囊周围炎。疾病确诊区域的活检可见毛囊间上皮呈银屑病样增生,或真皮下半部和皮下组织出现致密性混合炎性浸润。此外,可能出现慢性脓肿,内覆复层鳞状上皮的皮肤窦道,以及肉芽组织伴或不伴异物巨细胞。还可能出现毛囊皮脂腺单位破坏、纤维化,以及偶发的顶泌汗腺周围和外泌汗腺周围炎症。若临床特征提示鳞状细胞癌,也应实施活检。鳞状细胞癌可能表现为增长缓慢、坚实、非波动性、无溢液的肿块,其表面可受侵蚀或形成溃疡,累及慢性HS区域,尤其是肛周。超声检查可用于在术前评估是否存在窦道形成及其穿通范围及深度。核磁检查有助于显示肛门生殖区病变的范围。HS的诊疗也无需常规细菌培养。培养仅用于特定情况,例如临床表现提示为原发感染性疾病而不是HS、存在继发性蜂窝织炎等。目前尚无血清学检查可用于诊断HS。
诊断
目前我国尚无统一的诊断标准,参照欧洲皮肤病与性病学会及美国与加拿大HS基金会所制定的指南,本指南提出诊断要点如下,①病史:曾出现反复发作的疼痛性或化脓性皮损;②典型临床表现:腋窝、腹股沟、会阴、肛周及女性乳房下皱褶处等顶泌汗腺分布部位的深在疼痛性结节、脓肿、窦道、瘢痕;③HS/AI家族史;④皮损组织病理:早期可见毛囊口表皮细胞增生、角化过度,毛囊漏斗部淋巴细胞及组织细胞浸润;急性期真皮深层可见大量混合性炎症细胞浸润,常延伸至皮下组织,局部可见脓肿,并有窦道通向皮肤表面,窦道内包含炎症细胞和残余的角质,常见肉芽组织,伴炎症细胞及异物巨细胞;慢性期可见毛囊、皮脂腺和汗腺被破坏,伴广泛的纤维化。同时符合前2条即可诊断HS/AI,明确存在第3条可考虑家族性HS/AI,第4条对本病的诊断和鉴别诊断具有辅助作用。
鉴别诊断
HS/AI皮损表现为粉刺、丘疹、结节和囊肿时,需与寻常痤疮、疖、痈、丹毒、蜂窝织炎和表皮样囊肿等鉴别;皮损表现为脓肿、窦道和瘘管时,需与放线菌病、诺卡菌病、溃疡性皮肤结核、结节溃疡性梅毒、腹股沟肉芽肿、皮肤Crohn病、肛周脓肿和肛瘘、坐骨直肠窝脓肿等鉴别。长期溃疡性损害应注意排除皮肤鳞状细胞癌。结合典型部位的皮损分布特征及组织病理表现可鉴别诊断。
治疗
以Hurley分级Ⅰ、Ⅱ、Ⅲ级将病情严重程度分为轻、中、重度,临床上应根据不同病情严重程度选择不同的治疗方案。Hurley分级是1989年Hurley最早提出的HS/AI严重程度分级标准。Ⅰ级:单个或多个结节、脓肿,无窦道或瘢痕形成;Ⅱ级:单个或多个广泛散在的复发性结节、脓肿,伴窦道或瘢痕形成;Ⅲ级:整个受累区域弥漫分布多发、相互穿通的窦道和脓肿。此分级标准临床操作简便,应用最广泛,尤其适合临床分级和流行病学调查。但其分级中未采用量化的指标,主要以瘢痕和窦道等慢性损害作为指标,在判断治疗的有效性时并不敏感。
1.外用或局部注射治疗药物 外用药物主要适用于轻症患者,也可作为中、重度患者的辅助治疗。外用1%克林霉素溶液可减少细菌定植及伴发的炎症反应,用于脓疱等炎症性皮损,推荐每日2次,连续使用12周,注意有引起细菌耐药的风险;其他抗菌药物如氯己定、过氧化苯甲酰、鱼石脂等可作为备选。外用维A酸类、15%间苯二酚软膏等角质松解药物,可改善毛囊角化,缓解毛囊口阻塞。皮损内注射糖皮质激素(如5~10 mg/ml曲安奈德注射液0.2~2 ml,或复方倍他米松注射液)可迅速缓解急性炎症性皮损的疼痛与炎症反应,也可用于治疗顽固疼痛性结节,如果窦道处脓液细菌培养阳性则慎用糖皮质激素类药物。
2.系统治疗药物
(1)抗生素:系统应用抗生素适用于存在明显感染性炎症的患者。
一线治疗药物:口服四环素类抗生素,轻、中度患者的首选治疗,可单用或联合外用药治疗,推荐治疗方案为四环素(500 mg/次,每日2次)、多西环素(100 mg/次,每日2次)或米诺环素(50~100 mg/次,每日2次),建议连续使用12周,需注意四环素类抗生素不宜用于妊娠期、哺乳期女性及8岁以下儿童。
二线治疗药物:克林霉素与利福平联合治疗,适用于一线治疗无效的轻、中度患者,使用时需注意与其他药物间相互作用。
三线治疗药物:包括甲硝唑、莫西沙星、利福平,可选择三联治疗方案作为重度患者治疗的方案。推荐甲硝唑(500 mg/次,每日3次)、莫西沙星(400 mg,每日1次)联合利福平[300mg/次,每日2次,或10 mg/(kg·d)],疗程12周,甲硝唑口服6周需停药。
对于HS/AI局部感染经口服抗生素治疗无效,或合并系统性炎症反应综合征、血细菌培养阳性患者,可考虑厄他培南1g/d静脉输液治疗,或根据血培养与药敏结果选择其他敏感药物。厄他培南可作为重症患者的补救治疗或外科手术及其他长期维持治疗的过渡治疗选择,对于抗生素的使用周期与频率也应权衡抗生素耐药的风险。
(2)维A酸类:维A酸类药物可以减轻毛囊及皮脂腺导管上皮的过度角化,减少毛囊口角栓形成,具有抗炎、改善瘢痕的作用,但对HS/AI的疗效尚缺乏有效的证据。口服阿维A治疗适用于早期或慢性反复发作的患者,推荐剂量0.20~0.88 mg/(kg·d),连续使用3~12个月,育龄期女性需注意致畸风险。异维A酸仅推荐用于合并中、重度痤疮或常规治疗无效的HS/AI患者。
(3)生物治疗:近年来,随着生物治疗研究的进展,针对HS/AI不同靶信号分子的治疗药物包括TNF-α拮抗剂(阿达木单抗、英夫利西单抗、依那西普)、IL-17A拮抗剂(司库奇尤单抗)、IL-1拮抗剂(anakinra、canakinumab)、IL-12/23拮抗剂(乌司奴单抗)、IL-36抑制剂(spesolimab)、JAK抑制剂(upadacitinib, povorcitinib, tofacitinib),补体C5α抑制剂(IFX-1)及小分子靶向药物磷酸二酯酶4抑制剂(apremilast)已陆续进入临床应用,部分尚处于临床试验阶段。目前,我国尚无经国家药品监督管理部门批准应用于HS/AI治疗的生物制剂或小分子药物。国际上生物治疗主要适用于对系统应用抗生素等治疗无效的中、重度HS/AI患者。在我国使用生物治疗需严格掌握适应证,与患者充分沟通获得知情同意,并在使用期间注意相关不良反应,包括继发感染(如上呼吸道感染)、心血管事件、诱发肿瘤等。
阿达木单抗是全人源性抗TNF-α单克隆抗体,是经美国食品药品监督管理局批准用于治疗HS/AI的一线生物制剂。推荐方案:①第0周160 mg皮下注射,第2周80 mg皮下注射,随后40mg每周1次皮下注射,疗程12周;②40 mg每周1次皮下注射,疗程12周。英夫利西单抗是一种鼠/人嵌合型抗TNF-α单克隆抗体,为治疗HS/AI的二线生物制剂。 推荐方案:第0、2、6周5 mg/kg静脉注射,之后每2个月注射1次,治疗12周。一项共有633名HS/AI患者参与的临床试验发现,用药12周时阿达木单抗比安慰剂组有显著更高的临床缓解率(41.8% vs 26.0%,58.9% vs 27.6%),严重不良事件发生率相似。
此外,司库奇尤单抗(secukinumab)是人源化IL-17A单克隆抗体,目前欧洲已经批准用于本病的治疗,推荐方案:第0、1、2、3、4周每周300mg皮下注射,随后300mg每2周1次皮下注射,疗程16周。两项共有1084例HS/AI患者参与的临床试验发现,治疗16周时司库奇尤单抗治疗组的疗效显著优于安慰剂,持续用药52周后超过75%的患者保持了疗效。安全性无特殊。
近期有报道JAK抑制剂(upadacitinib, povorcitinib, tofacitinib)治疗本病临床症状得到改善,脓肿、炎性结节数量减少。一项开放性Ⅱ期临床研究显示第50天时75%的患者、第134天时83%的患者达到了HiSCR。
(4)系统应用糖皮质激素或免疫抑制剂:在病情急性发作或其他系统治疗的早期可短期系统应用糖皮质激素,推荐剂量:0.5~0.7 mg/(kg·d)泼尼松相当剂量为起始剂量口服,并根据病情改善逐渐减量。免疫抑制药物可抑制引起HS/AI发作的炎症级联反应,可作为抗生素、生物制剂治疗无效的难治性HS/AI的三线治疗方案。环孢素是一种T细胞免疫抑制药物,可作为长期控制炎症的一种选择,参考剂量:2~5 mg/(kg·d) ,治疗6周至7个月,使用时需注意其肾毒性、神经毒性、诱发高血压等不良反应。
(5)其他药物
1)抗雄激素药物:通过减弱和拮抗雄激素活性,减少皮脂腺分泌,改善毛囊角化,适用于具有以下1种或多种情况的女性HS/AI患者:①随月经周期疾病加重;②有痤疮样表现;③合并糖尿病、多囊卵巢综合征及雄激素过高者。醋酸环丙孕酮联合炔雌醇具有抗雄激素作用,可作为轻、中度或有高雄激素表现的女性患者的单一药物治疗,也可作为重度女性患者治疗的备选药物。
2)二甲双胍:具有改善胰岛素抵抗,减少胰岛素样生长因子1及其诱导产生的雄激素,适用于合并糖尿病、多囊卵巢综合征的女性患者,推荐剂量500 mg,每日2~3次口服。
3)氨苯砜:对于轻、中度患者还可选择氨苯砜口服,剂量25~200mg/d,疗程至少3个月,治疗时需监测患者血常规,对于葡萄糖-6-磷酸脱氢酶缺乏者需谨慎药物引起的溶血性贫血,检测HLA-B*13∶01等位基因有助于减少氨苯砜综合征的发生。
4)锌制剂:具有一定抗炎作用,抑制中性粒细胞趋化和角质形成细胞Toll样受体2的表达,口服葡萄糖酸锌可作为轻、中度HS/AI的二线治疗, 或局部或系统抗生素治疗的辅助治疗,推荐剂量90 mg/d,注意锌过量补充可能会抑制铜和铁的吸收。
5)秋水仙碱:能抑制中性粒细胞趋化,可联合抗生素或在维持治疗阶段单独使用,剂量0.5 mg/次,每日2次,疗程6~9个月,需注意药物可能引起的胃肠道反应、肌肉与周围神经病变及骨髓抑制。
6)沙利度胺:可抑制炎症细胞因子的表达,也可用于本病的治疗,参考剂量50~100 mg/d,疗程4个月以上,需注意致畸等不良反应。
3.物理疗法 激光治疗、光动力治疗、强脉冲光、射频治疗、放射治疗等可作为HS/AI的辅助或补充治疗。二氧化碳激光可以气化结节、脓肿和窦道,适用于中、重度HS/AI皮损的组织切除、减压及瘢痕修复。长脉冲1064 nm Nd:YAG激光具有对毛囊的选择性光热作用,可帮助清除皮损、减少复发,适应于中、重度HS/AI患者。光动力治疗是利用氨基酮戊酸代谢生成光敏物质原卟啉Ⅸ,经光照后产生化学反应,具有改善毛囊皮脂腺导管角化、抗菌及抗炎作用,临床报道治疗HS/AI有效。
4.手术治疗 手术治疗需根据疾病严重程度选择相应的手术方式。切开引流可缓解急性期HS/AI皮损的疼痛,适用于轻至中度患者。去顶术是一种针对复发性结节和窦道的有效治疗方式,适用于轻度散发性皮损或广泛分布的中、重度皮损。对于顽固难治性皮损可采用局部扩大切除术,扩大切除时首先要判断HS/AI累及的范围及深度,其次要判断是否累及肛管等重要组织器官。手术时须根据皮损累及的部位选择适当的麻醉方式,多数情况下应用改良膨胀麻醉技术即可满足手术需要。研究显示,沿窦道注射亚甲蓝有助于判断窦道走向与深度。手术过程中需彻底切除窦道及受累的软组织。切除术后可根据皮损的位置及面积选择二期愈合或一期闭合,缺损修复通常需根据缺损大小选择直接缝合、皮瓣修复及刃厚皮片移植等。
5.疼痛治疗 由于缺乏对HS/AI引起疼痛机制的研究,尚无特异性针对HS/AI疼痛的治疗方法。可选用局部止痛药物(如5%利多卡因凝胶、双氯芬酸凝胶)及非甾体抗炎药,治疗无效者可选用神经性止痛药(加巴喷丁、普瑞巴林)、曲马朵以及阿片类药物。
尽快控制疾病的炎症反应有利于缓解疼痛。
6.联合与分级治疗 HS/AI的治疗目的仍然在于降低发作频率和发作持续时间,减轻炎症反应,提高患者的生活质量。单一治疗方法很难完全控制HS/AI症状,需要多种方法联合治疗,且需根据疾病的严重程度采用不同的方法。推荐分级治疗方案见诊疗流程。
诊疗流程(图40-1)
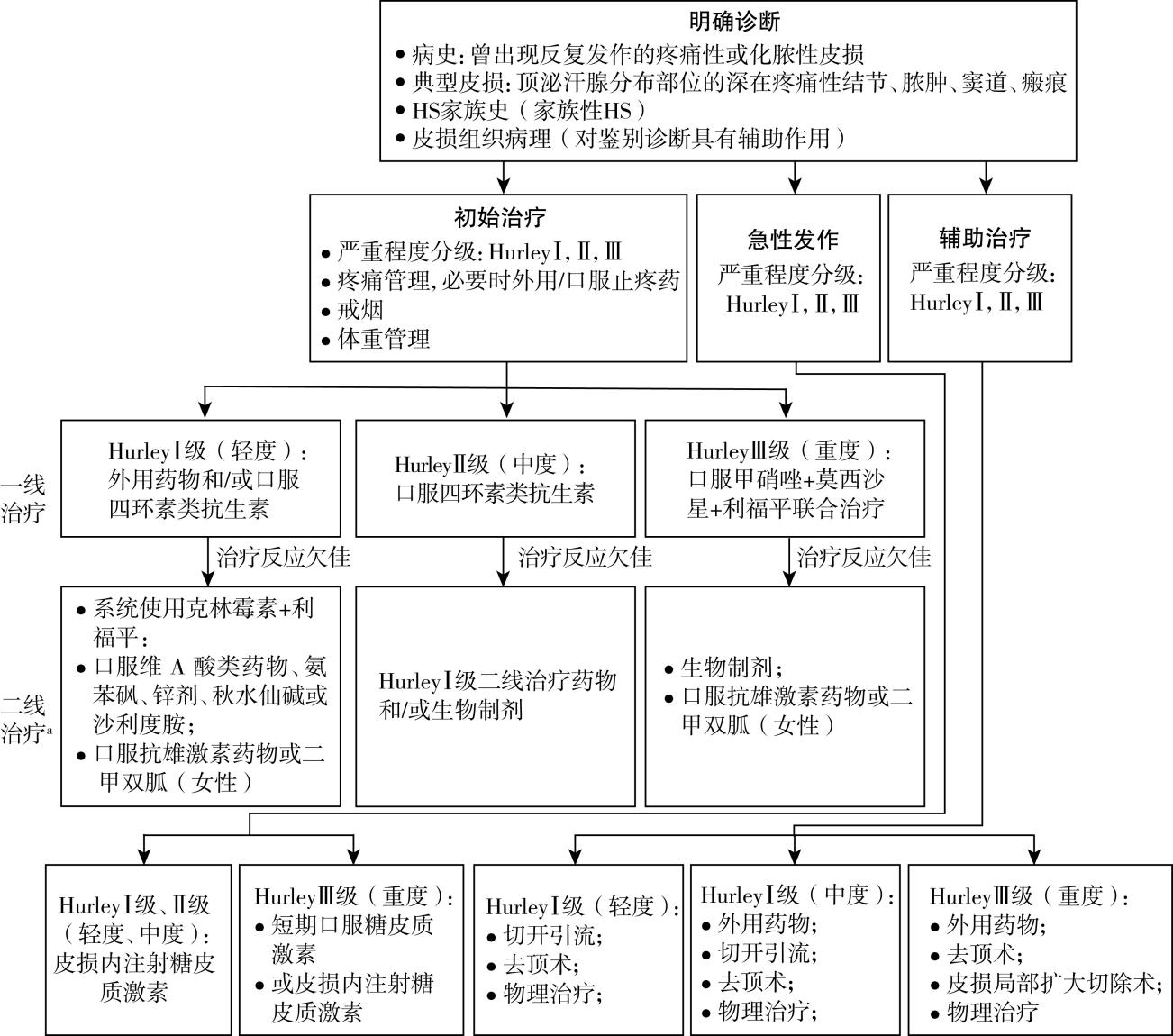
图40-1 化脓性汗腺炎诊疗流程
注:二线治疗包括多种药物,基于目前的临床证据,无优先推荐,可根据患者具体情况单独或联合使用
参考文献
[1]Garg A, Kirby JS, Lavian J, et al. Sex⁃and age⁃adjustedpopulation analysis of prevalence estimates for hidradenitis suppurativa in the United States. JAMA Dermatol,2017,153(8):760-764. [2]Lee JH, Kwon HS, Jung HM, et al. Prevalence and comorbidities associated with hidradenitis suppurativa in Korea: a nationwide population⁃based study. J Eur Acad Dermatol Venereol,2018,32(10):1784-1790.
[3]Wang Z S , Li J , Ju Q , et al. Prevalence of acne inversa (hidradenitis suppurativa) in China: a nationwide cross-sectional epidemiological study. Int J Dermatol Venereol,2022,5(1):1-7.
[4]Wang B, Yang W, Wen W, et al. Gamma-secretase gene mutations in familial acne inversa. Science,2010,330(6007):1065.
[5]Ring HC, Thorsen J, Saunte DM, et al. The follicular skin microbiome in patients with hidradenitis suppurativa and healthy controls. JAMA Dermatol,2017,153(9):897 -905.
[6]van der Zee HH, Jemec GB. New insights into the diagnosis of hidradenitis suppurativa: clinical presentations and phenotypes. J Am Acad Dermatol,2015,73(5 Suppl 1):S23-S26.
[7]Zouboulis CC, Desai N, Emtestam L, et al. European S1 guideline for the treatment of hidradenitis suppurativa/acne inversa. J Eur Acad Dermatol Venereol,2015,29(4):619-644.
[8]Alikhan A, Sayed C, Alavi A, et al. North American clinical management guidelines for hidradenitis suppurativa: a publication from the United States and Canadian Hidradenitis Suppurativa Foundations: Part I: diagnosis, evaluation, and the use of complementary and procedural management. J Am Acad Dermatol,2019,81(1):76-90.
[9]Kimball AB, Okun MM, Williams DA, et al. Two phase 3 trials of adalimumab for hidradenitis suppurativa. N Engl J Med,2016,375(5):422-434.
[10]Kimball AB, Jemec GBE, Alavi A, et al. Secukinumab in moderate-to-severe hidradenitis suppurativa (SUNSHINE and SUNRISE): week 16 and week 52 results of two identical, multicentre, randomised, placebo-controlled, double-blind phase 3 trials. Lancet,2023,401(10378):747-761.


