157、骨巨细胞瘤
罕见病诊疗指南(2025年版)
概述 骨巨细胞瘤(giant cell tumor of bone,GCTB)是一种原发于骨骼的交界性肿瘤,主要由多核巨细胞和单核细胞组成。该疾病常发生在20到40岁的成年人,尤其是女性。骨巨细胞瘤多数位于长骨骨端。在临床上,该疾病具有局部侵袭性,可局部复发和远处转移。
病因和流行病学
骨巨细胞瘤的确切发病机制并不清楚。90%~96%的骨巨细胞瘤会出现H3F3A突变,突变类型包括p.G34W,p.G34L,p.G34R和p.G34V等,极少数为野生型不发生突变。
骨巨细胞瘤的溶骨过程一般认为是通过RANK-RANKL通路的激活诱发。骨巨细胞瘤在病理形态上主要有两种细胞:单核细胞和破骨细胞样多核巨细胞。其中,单核细胞又分两类,一类是梭形基质细胞,另一类是单核巨噬细胞样细胞。梭形基质细胞是骨巨细胞瘤的肿瘤细胞,具有增殖潜能。单核巨噬细胞样细胞是破骨细胞样细胞的前体,它们聚集融合而成为破骨细胞样多核巨细胞。破骨细胞样巨细胞表达RANK,而梭形基质细胞表达RANKL,RANKL与RANK结合,从而激活RANK-RANKL通路,产生溶骨过程。
骨巨细胞瘤属于罕见病,年发病率约为(1.2~1.7)/100万。不同国家和地区报道的发病率可能并不相同。在欧美,骨巨细胞瘤占所有原发骨肿瘤的3%~5%,但我国骨巨细胞瘤占所有原发骨肿瘤的13.7%~17.3%。在美国,男女发病人数比例约为0.8∶1,而我国男女发病人数比例为(1.26~1.77)∶1。骨巨细胞瘤可发生于任何年龄,但常见于20~40岁。
临床表现
骨巨细胞瘤的主要症状是疼痛,疼痛通常呈缓慢发展并逐渐加重的特点。疼痛的持续时间从最初出现到就诊可以为1~6个月,有些甚至长达18个月。与此同时,患者很少出现发热等全身症状。
在肢体部位的骨巨细胞瘤,除了疼痛之外,患者的邻近关节可能会出现肿胀和肿块。随着肿块的增大,患处的皮温可能会有所上升。这种肿瘤通常发生在长骨的骨端,靠近关节,当它增大时,可能会限制关节的活动。若不进行治疗,肿瘤可能持续增大,进而增加病理性骨折的风险。对于未经及时治疗的肿瘤,可能需要更为激进的手术方法来进行治疗。
脊柱和骶骨的骨巨细胞瘤往往引发神经系统的症状,主要体现为疼痛,尤其是在负重或行走时疼痛加重。若不及时治疗,疼痛可能会进一步加重,甚至可能发生病理性骨折,从而导致下肢的感觉和运动功能受损。特别是骶尾部的骨巨细胞瘤,可能会影响排尿和排便功能。而骨盆部位的骨巨细胞瘤,其症状可能较为隐匿,但当其影响到骨强度时,患者可能会体验到局部疼痛。
辅助检查
骨巨细胞瘤的辅助检查主要是影像学,X线检查能显示病灶的轮廓,而肿瘤通常呈现为偏心性溶骨、膨胀性改变。在长管状骨中,这种肿瘤多发生在干骺端。增强CT可以显示骨破坏的情况和肿瘤的血运状况,而增强MRI对于显示软组织包块和骨髓腔内的侵犯范围则更为清晰。
进行分期检查时,一般会推荐胸部CT平扫和全身骨扫描,这是为了发现可能的肺部转移瘤和骨的多中心病灶。PET-CT作为功能性的成像检查,可以反映肿瘤部位的代谢活跃程度,从而用于疗效评估。
当考虑到转移病灶的影像学检查时,由于肺部是骨巨细胞瘤最常见的转移部位,胸部CT平扫通常是首选。而其他可能的转移部位,例如腹部、盆腔和脑,都可以选择相应的CT或MRI进行评估。对于骨部的转移病灶,X线检查也是推荐的。
常规的实验室检查,如碱性磷酸酶和血沉,一般在正常范围内。
诊断
骨巨细胞瘤的诊断是在临床和影像学诊断的基础上进行穿刺活检病理组织学确诊,即使临床和影像学都显示骨巨细胞瘤的典型表现,活检仍然是必要的确诊手段。
骨巨细胞瘤显微镜下常见多少不等的多核巨细胞及增生的单核细胞,骨巨细胞瘤组织学常有异质性。经典骨巨细胞瘤由无明显异型性的单核细胞和多核巨细胞组成,同时可以合并有坏死出血,灶片状纤维组织增生及黄瘤样组织细胞,反应骨/化生骨和软骨的出现,合并动脉瘤样骨囊肿等情况均不少见。坏死、单核细胞轻度异型性、丰富的核分裂象、脉管内瘤栓等都不提示恶性,与骨巨细胞瘤整体预后无关。
推荐使用免疫组化抗体H3G34W来协助骨巨细胞瘤诊断。同时也可以完善H3K36M、SATB2、Ki67、RANK、RANKL、SMA、P53、P16、CD68、P63等其他免疫组化来帮助诊断与鉴别诊断。
鉴别诊断
常见的需要与骨巨细胞瘤鉴别诊断的疾病包括:
1.软骨母细胞瘤 虽然软骨母细胞瘤也好发于骨端并可出现巨细胞,但这种肿瘤的主要特点是由均一的、密集排列的圆形/卵圆形软骨母细胞伴软骨样基质构成,软骨基质常发生钙化呈鸡笼样/格子样。软骨细胞胞质嗜酸性,常见核沟。分子遗传学方面,软骨母细胞瘤常有H3F3B基因突变,与骨巨细胞瘤常伴随的H3F3A基因突变不同,可通过IHC,PCR,一代或二代测序检测。
2.动脉瘤样骨囊肿 原发动脉瘤样骨囊肿由充满血液的囊腔构成,纤维间隔由无明显异型性的成纤维细胞,散在的多核巨细胞,毛细血管以及新生反应骨构成。70%~75%动脉瘤样骨囊肿常伴随USP6基因重排,不存在骨巨细胞瘤常见的H3FA突变。旧称为继发性动脉瘤样骨囊肿(现称伴有动脉瘤样骨囊肿样结构)不存在c基因重排。
3.富巨细胞骨肉瘤 较为罕见的骨肉瘤亚型,肿瘤组织中可以富含巨细胞,但异型性明显的单核肿瘤细胞和明确的肿瘤性成骨是诊断的关键,H3F3A分子和蛋白水平检测也是有效鉴别手段。
4.棕色瘤 棕色瘤是由于过度分泌甲状旁腺激素引起的骨病变。常为多发。镜下见骨小梁呈隧道样或切割样吸收,骨表面可见大量破骨细胞,附近髓腔纤维化及新生编织骨形成。破骨细胞重吸收产生多个相互交通的囊性区域伴多量含铁血黄素沉积而呈棕色。分子检测缺乏特异性基因改变。
5.非骨化性纤维瘤 这是一种青少年好发的良性骨病变,由梭形成纤维细胞样细胞呈storiform排列,散在分布多核巨细胞,可见含铁血黄素沉积及泡沫细胞聚集。部分病例可以检测到KRAS基因和FGFR1基因改变,少许病例还伴有NF1胚系突变。
6.巨细胞修复性肉芽肿 颅面骨常见,它的组织学特点是含有较多量的多核巨细胞与梭形纤维母细胞样细胞,但与骨巨细胞瘤相比,这些巨细胞分布更为广泛,并且伴随有大量的出血和新生血管。缺乏骨巨细胞瘤特异性的H3F3A基因突变。
治疗
骨巨细胞瘤最主要的治疗方法是外科手术。由于其转移和多中心病灶引起的死亡发生率相对较低,控制局部复发成为了临床治疗的核心目标。根据肿瘤的具体情况,可分为整块切除和病灶内刮除两种手术方法。大量病例表明,整块切除的复发率在1.6%~12%,而病灶内刮除的局部复发率则为10%~65%。但随着外科技术的进步,局部扩大刮除的复发率已降低至10%以下,病灶内刮除仍然是首选的手术方法。
对于不可切除的骨巨细胞瘤,地舒单抗药物治疗被推荐为主要治疗手段,在骨巨细胞瘤中,采用剂量每次120mg,皮下注射,第1,8,15,28天给药,后每28天给药1次。尤其是对于那些没有手术机会的患者,长期使用地舒单抗可以有效控制疾病进展、缓解或消除相关症状。对于手术困难预期经药物治疗后可以转为可切除的骨巨细胞瘤,选择地舒单抗主要是在手术前使用。这种应用旨在降低肿瘤的血供,使得肿瘤的边界更加清晰,进而降低手术的难度。在应用地舒单抗治疗后,医生需要定期评估药物治疗的效果。经过药物治疗后选择的手术方案可能相较于治疗前更少地损害患者的功能,从而起到疾病降期的效果。
在某些情况下,放射治疗(RT)仍然是一个有价值的治疗选项。放射治疗被应用与手术结合或者单独应用,尤其在患者存在不可切除和/或复发性疾病时,以提高局部控制率和疾病无进展生存率(DFS)。然而,放疗有一定的副作用风险。考虑到骨巨细胞瘤属于非恶性肿瘤,使用放疗应当比恶性肿瘤有更高的风险意识。因此,一般建议,只有在没有其他治疗选择时,才应考虑放射治疗。
选择性动脉栓塞(SAE)是一种特定的治疗方法,主要是通过选择性地将动脉导管和栓塞剂导入到指定的动脉,从而阻断肿瘤的供血,达到缩小或控制肿瘤生长的效果。对于位于骨盆、脊柱和骶骨等部位的不可切除病灶,选择性动脉栓塞治疗有一定价值。它不仅可以作为手术的辅助治疗,减少术中出血,降低手术的风险。对于不可切除的肿瘤,反复进行选择性动脉栓塞治疗可以有效地控制和稳定肿瘤的生长。
并发症监测
对骨巨细胞瘤患者进行定期监测是至关重要的,以便及时发现并处理任何可能的并发症,包括局部复发、远处转移及骨的多中心病灶。首先,应定期进行体格检查,根据临床需要,对手术部位进行影像学检查,包括X光、CT扫描和MRI(必要时选择增强)。鉴于转移的平均时间为2~4年,因此应每6~12个月进行一次胸部影像学检查,持续4年,之后每年进行一次,或根据临床需要进行。如出现复发疾病(无论是局部还是转移性),应根据初次诊断时的局部疾病或转移疾病进行管理。
诊疗流程(图36-1)
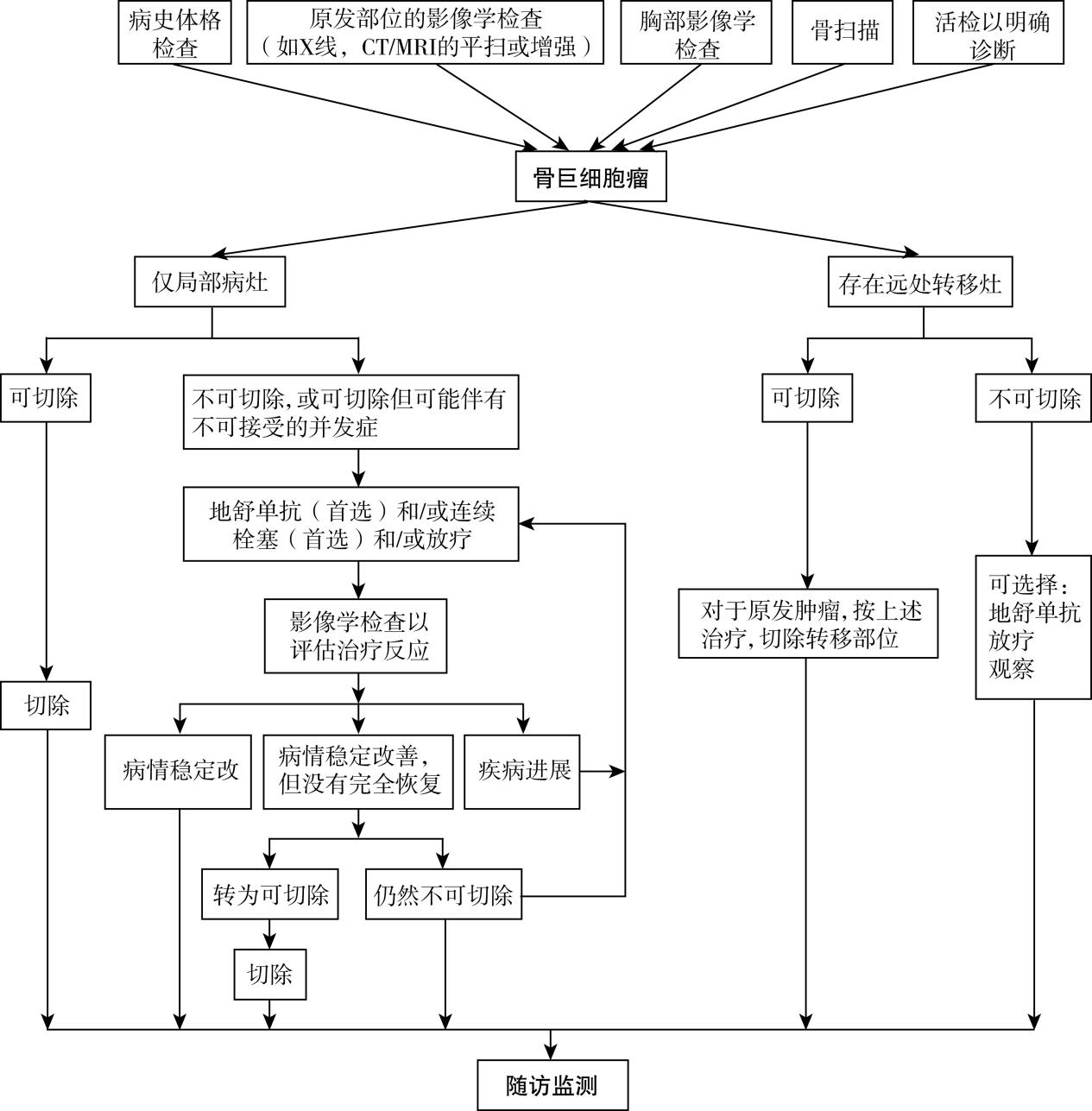 图36-1 骨巨细胞瘤诊疗流程
图36-1 骨巨细胞瘤诊疗流程
参考文献
[1] Niu X, Zhang Q, Hao L, et al. Giant cell tumor of the extremity. J Bone Jt Surg,2012,94(5):461-467.
[2] Campanacci M, Baldini N, Boriani S, et al. Giant-cell tumor of bone. J Bone Jt Surg Am volume,1987,69(1):106-114.
[3] Sung H, Kuo D, Shu W, et al. Giant-cell tumor of bone: analysis of two hundred and eight cases in Chinese patients. The Journal of Bone and Joint Surgery American Volume,1982,64(5):755-761.
[4] Montgomery C, Couch C, Emory C, et al. Giant cell tumor of bone: review of current literature, evaluation, and treatment options. The Journal of Knee Surgery,2019,32(4):331-336.
[5] Chawla S, Blay J-Y, Rutkowski P, et al. Denosumab in patients with giant-cell tumour of bone: a multicentre, open-label, phase 2 study. Lancet Oncol,2019,20(12):1719-1729.


