143、隆突性皮肤纤维肉瘤
罕见病诊疗指南(2025年版)
概述 隆突性皮肤纤维肉瘤(dermatofibrosarcoma protuberans,DFSP)是一种罕见的局部侵袭性成纤维细胞肉瘤,起源于真皮软组织,并累及皮下组织、筋膜、肌肉甚至骨骼,一般无包膜。本病于1924年由Darier和Ferrandh首次报道。DFSP临床表现为躯干或四肢缓慢进展、无痛性红斑或紫癜性斑块(通常需要数年),手术切除后易复发(复发率约20%)、发生远处转移风险较低;组织学表现为梭形细胞呈典型的席纹状或车辐状排列。诊断主要依靠组织病理学检查。广泛局部切除(wide local excision,WLE)和Mohs显微外科手术(Mohs micrographic surgery,MMS)仍是目前治疗DFSP的最有效方式,以伊马替尼为代表的分子靶向治疗、氩氦刀冷冻消融术及局部放疗在治疗不可切除或部分可切除的肿瘤,预防局部复发等情况下仍具有应用价值。
病因和流行病学
DFSP约占所有恶性肿瘤的0.1%,约占所有软组织肿瘤的1.8%~6%。DFSP的发病率约为(0.8~5)/100万。DFSP可发生于任何年龄段,常见于青年和中年人,20~50岁为发病高峰期,在40~50岁左右达到顶峰,此后发病率逐渐下降,儿童患者仅占所有DFSP病例的6%,低于成人。男女发病率相当。所有种族均可发生DFSP,黑人发病率高于白人,约为白人的1.5~2倍。
DFSP的发病机制尚不完全清楚。DFSP具有特殊的细胞遗传学异常,主要为染色体结构异常,超过90%被诊断为DFSP的患者携带t(17;22)(q22;q13)易位。染色体t(17;22)易位重排及含有17号和22号染色体序列的环状染色体形成,两者均导致相同的分子结构重排,使17q21-22的1型胶原蛋白α1基因(COL1A1)和22q13.1的血小板衍生生长因子-β多肽基因(PDGFB)融合,产生特异性COL1A1-PDGFB融合基因,促使COL1A1启动子激活正常情况下被抑制的PDGFB基因。COL1A1-PDGFB所产生的融合蛋白经过加工后形成功能齐全的PDGFB,与其受体(platelet derived growth factor receptor-β,PDGFR-β)结合后,导致PDGF功能失调,持续激活下游信号通路RAS-MAPK和PI3K-AKT-mTOR,最终通过促进细胞过度增殖而导致肿瘤发生。此外,还有报道5号、8号染色体三体性,以及其他易位类型如t(X;7)(q21.2;ql1.2)平衡易位,t(2:17)(q33;q25)和t(9;22)(q32;ql2.2)等。隆突性皮肤纤维肉瘤中病灶处p53基因过表达常伴随较高的增殖活性和非整倍性。
临床表现
DFSP最常见于躯干和四肢近端(肩部和骨盆区域),50%~60%的DFSP发生于躯干,20%~30%发生于四肢近端,10%~15%发生于头颈部,外阴、乳腺则少见。皮损发生在头颈部的病例,复发率很高(50%~75%)。DFSP早期临床表现常为缓慢生长的硬斑块或小结节,颜色接近正常皮肤,无明显自觉症状,后期随肿瘤的缓慢增大,瘤体可逐渐凸起、变硬,最终可形成紫色至棕红色结节和肿物,直径1cm至数厘米不等。周围皮肤的毛细血管可出现扩张。触诊皮损坚实,与皮下组织粘连。
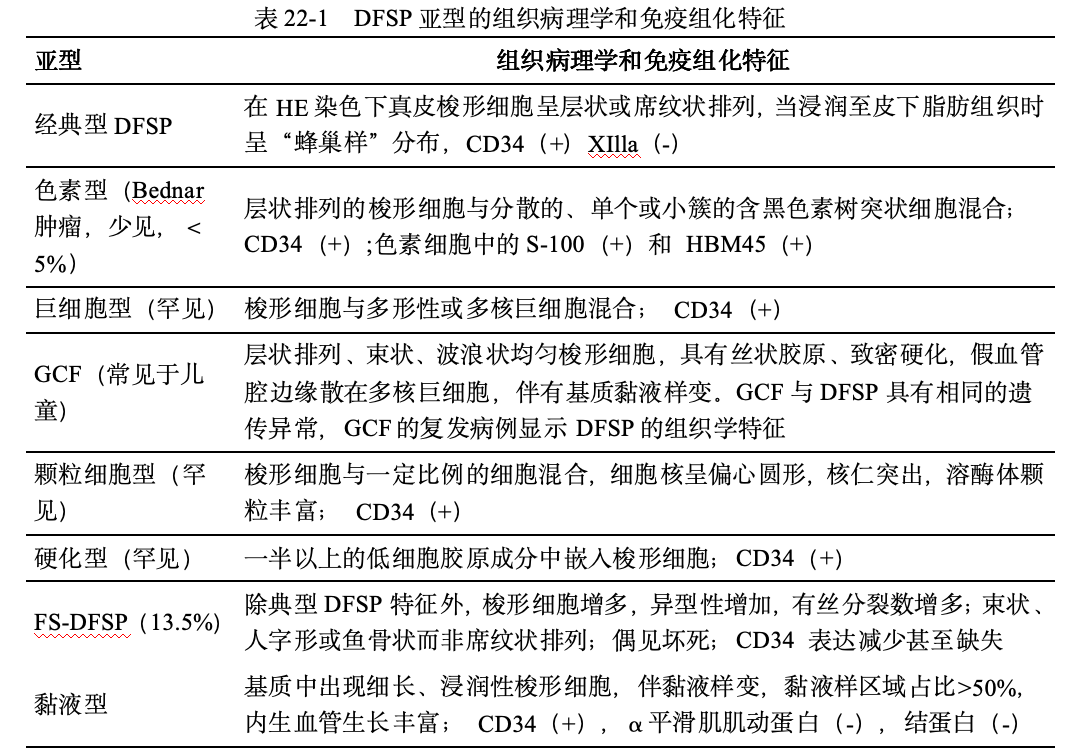
在组织病理学上,经典型DFSP以席纹状排列为特征,常浸润至皮下脂肪组织。除经典型DFSP外,常见亚型包括色素型(也称Bednar瘤)和纤维肉瘤型(fibrosarcomatous DFSP,FS-DFSP),前者肿瘤内可见多少不等的色素性树突状细胞,后者瘤细胞失去席纹状结构而成长条束状或鱼骨样排列,类似纤维肉瘤。少见亚型包括黏液样型、萎缩型和斑块型、肌样、硬化型、颗粒细胞型和混杂型等。在所有亚型中,只有纤维肉瘤型恶性程度高,局部复发和远处转移的发生率较高。
1.Bednar瘤 约有不到5%的DFSP内含有向黑素细胞或黑素细胞-施万细胞分化的细胞,这些细胞能生成黑色素,被称为Bednar瘤,又称为黑色素型DFSP。Bednar瘤与一般DFSP具有相似的临床特征和遗传学特性。从组织学看,通过含有黑色素的树突状细胞可与普通型DFSP相区分。
2. 巨细胞纤维母细胞瘤样型(giant cell fibroblastoma,GCF) GCF是一种少见的肿瘤,几乎仅发生在20岁之前,现认为GCF是DFSP的幼年型。它与DFSP在临床特性及组织学特征上存在诸多共同之处:均发生在真皮、有类似的局部侵袭性生长过程、易复发;与DFSP具有相似的染色体核型和分子重排。
3.FS-DFSP 该型约占所报道DFSP总数的10%,以在DFSP中包含一定数量的纤维内瘤样区域为特征。在细胞遗传学及分子水平,DFSP中纤维肉瘤样区域与纤维肉瘤型DFSP极为相似。
4.颗粒细胞型DFSP 颗粒细胞样变是一种非特异性的退行性变,可见于多种肿瘤。颗粒细胞型DFSP极少见,仅有数例报道。与一般DFSP在组织学上有一定相似性。
辅助检查
1.皮肤镜检查 2013年,Bernard等提出6种典型DFSP在皮肤镜下的表现:精细色素网(87%),血管(80%),无结构的浅棕色区域(73%),亮白色条纹(67%),粉红色背景色(67%)和无结构的低色素或脱色区域(60%)。所有典型DFSP均至少存在上述2种皮肤镜表现,87%存在上述3种表现,且33%同时存在这6种表现。
2.影像学检查 包括超声、CT和磁共振(MRI)等。因其为浅表软组织肿块,故首选超声检查用于DFSP的初步评估。在超声下DFSP表现为皮下低回声结节状肿物,边界清楚,形态规则,内部血流丰富,不伴局部淋巴结肿大,内部有时会出现杂乱回声。需要与皮肤纤维组织细胞瘤(cutaneous fibrous histiocytoma,FH)、浅表脂肪瘤和血管瘤等良性病变进行鉴别。当怀疑肿瘤累及筋膜内或下方结构时,建议进行活检前影像学检查。DFSP确诊后术前可行MRI及CT检查以帮助了解肿瘤浸润范围和深度,以及肿瘤与正常解剖结构的关系,对肿瘤进行分期,从而确定手术切除范围。DFSP很少出现淋巴或血行转移。如果出现远处转移,肺部是最常见的部位,因此患者有必要行术前胸部X线片或CT检查,尤其是晚期DFSP、复发或者含纤维肉瘤成分的患者更应该行此类检查,以排除肿瘤肺部转移风险。有研究表明MRI是术后随访的第一选择,复发性DFSP在MRI上多表现为结节状、均质、边界清晰,并有明显的对比增强。
3.组织病理学 组织病理学检查仍是诊断DFSP的主要手段,其病理特征为肿瘤位于真皮内及皮下,“蟹足样”浸润生长,呈“席纹状”排列、“轮辐状”或“车轮状”结构,主要由弥漫的异型梭形细胞构成,在胶原纤维和结缔组织间浸润生长,一般情况下会浸润周围的真皮和脂肪组织,瘤细胞多沿脂肪小叶间隔浸润,并形成特征性的蜂窝状浸润结构。
早期斑块状损害的特点是表面扁平,细胞成分少,浸润细胞呈细长梭形,排列成长束状与表皮平行。细胞散布于纤细的胶原纤维间,呈蜂窝状或波浪状浸润。细胞核无明显异型,核分裂象少见。浸润可累及附属器,导致附属器的破坏消失。浸润的梭形细胞也可累及皮下组织,常呈多层状模式。
随着肿瘤发展至结节期,细胞成分逐渐增多,这些细胞呈“席纹状”排列,累及皮下组织呈“蜂巢样”模式。细胞核染色质浓集,核分裂象常见。结节内可出现黏液样区域,在血管黏液性基质内大量圆形至星形的细胞浸润具有特征性。分化差的纤维肉瘤病灶内细胞成分更多,这些细胞束状交叉排列呈“鱼骨样”,细胞的异型及核分裂更加明显。
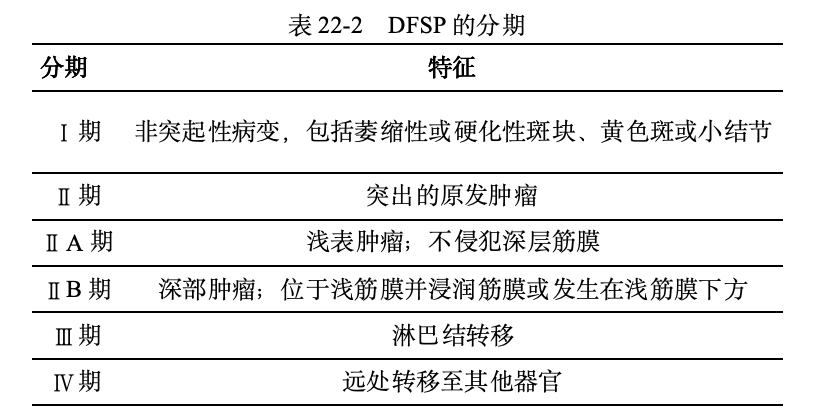
DFSP特征性表达CD34(+),其他免疫学标志物还包括波形蛋白(+)、P75(+)、平滑肌肌动蛋白(-)、结蛋白(-)、角蛋白(-)、S-100(-)等,但这些指标特异性都不高。对于色素型DFSP,S-100(+)是其主要的标志。Ki-67增殖指数是唯一的独立预测因子,高Ki-67指数意味着高复发率(表22-1,表22-2)。
诊断
经典型DFSP早期进展缓慢,临床症状不明显(孤立的斑块,质地坚硬,周围有红色、棕色或正常皮肤)、皮肤损害特异性低,易被患者忽视,且易与皮肤纤维组织细胞瘤等相混淆,造成漏诊、误诊。临床上,约52%的患者被误诊为表皮囊肿、脂肪瘤、良性纤维瘤、瘢痕疙瘩或其他疾病。因此,全面的病史和体格检查,以及皮肤镜检查、影像学检查等辅助检查非常重要。组织病理学是诊断DFSP的金标准,对于所有疑似病例,应进行活检以诊断。染色体检查可发现大部分患者有t(17, 22)染色体异位。
鉴别诊断
由于DFSP的形态和免疫特征与多种其他梭形细胞肿瘤重叠,因此其鉴别诊断范围广泛。斑块期DFSP病理学上需和萎缩性皮肤纤维瘤、皮肤肌纤维瘤、结缔组织痣和神经瘤相鉴别。结节期DFSP须与扩展至皮下组织的深在性皮肤纤维瘤、纤维肉瘤和恶性外周神经鞘瘤相鉴别。先天性和儿童期DFSP表面萎缩,和/或色素减少呈蓝红色,后者可能被误诊为血管畸形或血管肿瘤。DFSP的遗传特征为t(17;22),COL1A1-PDGFB融合转录物,是DFSP与其他具有类似组织学表现的肿瘤相鉴别的有用方法。
浅表型(特别是真皮的)DFSP与勋章样真皮树突状细胞错构瘤(斑块状CD34+真皮纤维瘤)的临床病理诊断标准有重叠。但后者FISH或RT-PCR检测未发现染色体t(17;22)不平衡交互易位,真皮乳头和邻近的真皮网状层上部可见带状CD34+成纤维细胞增生,为了诊断和鉴别诊断的需要,病理取材标本应包含足够的皮下组织。
由于DFSP与FH形态学相似而极易混淆,但二者在治疗上却完全不同,需要准确的诊断标志物对二者进行鉴别,目前临床常用的免疫组化标志物为CD34和FⅩⅢa。DFSP通常免疫学表型为CD34阳性,FⅩⅢa阴性,在斑块期,梭形细胞CD34强阳性,斑块区内比结节区更强,借此可与巨大型和/或多细胞型FH相鉴别。超声上,FH多表现为内部血流相对稀少,有时甚至没有,内部回声比较单一。
治疗
手术切除是目前治疗DFSP的最有效方式。DFSP具有局部浸润和容易复发的特点,即使手术切缘为阴性,手术切除后局部复发率仍较高,辅助放疗和靶向治疗可降低该病局部复发和转移的发生率。因此,对于局部晚期或转移性病例,建议进行以伊马替尼为代表的分子靶向治疗、氩氦刀冷冻消融术及局部放疗。DFSP需要终生监测复发情况,大多数复发的发生在初次切除后3年内,发生局部复发的中位时间估计为32个月。
1.手术切除 是DFSP的标准和首选治疗方法。由于肿瘤细胞的侵袭性生长、“微浸润”现象、不规则的边缘、伪足样延展特性,深部浸润范围远大于体表所见面积。使手术范围的确定变得非常困难,容易造成术者对肿瘤边界及浸润深度的误判,出现切缘不净、手术耗时长等现象,手术必须尽可能地将肿瘤彻底切除、避免复发,初次手术切除不彻底是本病复发的重要因素。DFSP的淋巴转移罕见,术中无须做预防性的区域淋巴结清扫。如果术前彩超提示区域淋巴结肿大,可行淋巴结病理检查,阳性者行淋巴结清扫术。对于局限性的DFSP,可行手术完整切除,包括广泛局部切除(WLE)和Mohs显微外科手术(MMS)2种方式。因需行扩大切除,如手术缺损范围较大,尤其是颜面部等损容性的缺损,术中应考虑创面美容修复,可通过邻近皮瓣成形术或植皮手术闭合创面。
(1)WLE:推荐切除距离肿瘤边缘2~4cm的正常组织、基底部深筋膜,深度达肌肉表面或颅骨膜,以彻底切除病灶,获得阴性切缘。术前行MRI检查,如果累及肌肉则须将其一并切除。对于复发的肿瘤,尽可能要使切缘距离肿瘤5cm以上,同时切除肿瘤周围及基底部受累的组织。
(2)MMS:与局部广泛切除相比,MMS是治疗较小的DFSP的首选手术方法,基本方法是将肿瘤及其周围组织分层连续切除,每切除一层均送组织病理学检查,因此,MMS手术相较于WLE手术可最大限度地保留面部等解剖学敏感区域的正常组织,有更高治愈率、清除率、更低局部复发率和最大组织保护,可在缺损重建前完成边缘的全面病理学检查。
2.化学治疗 目前普遍认为传统化疗对DFSP无效。甲磺酸伊马替尼是一种特异性酪氨酸激酶抑制剂,可以阻滞PDGFR-β,已成为第一种全身治疗DFSP的有效靶向药物,其缓解率约为50%~60%。伊马替尼治疗DFSP主要有两方面作用:①抑制癌基因激活信号通路(PDGF信号通路),诱导细胞凋亡;②上调抗原呈递作用,使肿瘤浸润在细胞毒性T淋巴细胞中,诱导其凋亡。
目前FDA已批准伊马替尼用于局部晚期或不能切除、术中无法行充分扩大切除或术后切缘为阳性、远处转移或复发的成人DFSP患者的替代治疗;也可作为新的辅助治疗药物在术前使用,以缩小瘤体的体积,便于手术切除,提高手术的有效性。伊马替尼起始剂量为400 mg/d或800 mg/d时对局部晚期或转移性DFSP的治疗同样有效,两种起始剂量的疗效无明显差异。由于患者对较低剂量的耐受性更好,且不良反应较少,DFSP的欧洲指南建议以400 mg/d作为起始剂量。
缺乏染色体易位t(17;22)的患者通常对伊马替尼没有反应。有染色体易位的FS-DFSP患者虽然对伊马替尼有反应,但是会很快出现耐药性,故手术不能根治或伊马替尼治疗失败或耐药的患者应建议使用蒽环类药物治疗。其他的酪氨酸激酶抑制剂如舒尼替尼和索拉非尼可能对治疗DFSP也有一定效果,但目前关于其临床用药经验十分有限。
3.放射治疗 DFSP对放疗敏感。单独使用放疗可作为原发性DFSP、切除范围有限的病变提供更高的治疗效益,但仅在极少数情况下将其作为初始治疗,临床上大多采用手术联合放疗的方式,将放疗作为DFSP术前或术后治疗的有效补充。针对肿瘤体积较大或无法直接切除的病变,可接受术前放疗,待肿瘤缩小后再行手术。对于术后病理提示切缘阳性、紧邻肿瘤边界及解剖部位受限者,当其存在肿瘤体积大、复发、手术切除范围大及可疑FS-DFSP等条件时均须接受术后放疗,以避免再次手术并造成正常组织丢失过多。一般建议在术后3~4周伤口愈合后行放疗。推荐切缘阳性或可疑切缘者的放射剂量为50~60 Gy,在临床条件允许时,可外扩3~5 cm进行放疗,预防局部复发。
4.氩氦刀冷冻消融术 冷冻消融作为一种治疗肿瘤的微创技术,具有操作简单、组织创伤小、患者耐受性好等优点,是治疗皮肤恶性肿瘤的一种重要方式。冷冻消融术可以作为一种治疗DFSP的相对安全和有效的技术。氩氦刀冷冻消融具有消融边界清晰、无痛、可同时消融多个病灶等优点,其可直接破坏肿瘤组织,而且坏死细胞的产物可刺激和诱导机体产生抗肿瘤免疫反应。术后患者可能出现轻微不良反应,如发热、局部水肿、轻度神经损伤和局部疼痛等。单次冷冻消融治疗后的局部复发率较高,经过多次冷冻消融治疗后患者的术后局部复发率降低。
5.其他方法 全反式维A酸(ATRA)可通过RARα、RARβ2条通路抑制DFSP细胞的增殖,为临床应用维A酸类药物辅助治疗手术难以切除或复发转移的DFSP病例提供了初步理论依据。抑制血管内皮生长因子(VEGFR)的阿帕替尼联合化疗可能是治疗DFSP的潜在方式,但仍需要大规模的前瞻性临床试验加以佐证。
预后
局部复发是手术切除后的主要问题。切缘阳性情况下,局部复发的概率范围为20%~50%,FS-DFSP或多形性肉瘤超过50%的患者出现局部复发,并且通常会多次复发。不到5%的患者会发生转移,FS-DFSP或多形性肉瘤10%~15%发生转移。肺部是远处转移最常见的部位,而淋巴结转移很少见。手术广泛切除后且镜下切缘阴性,DFSP的预后通常良好。充分的局部控制和清晰的手术切缘可以减少局部复发和转移的发生率。年龄增加、有丝分裂指数高、切缘阳性和细胞结构增加是临床结果不佳的预测因素。局部复发的中位时间约为32~38个月,必须进行长期临床随访。建议前五年每隔6~12个月进行监测,此后每年进行一次评估。
诊疗流程(图22-1)
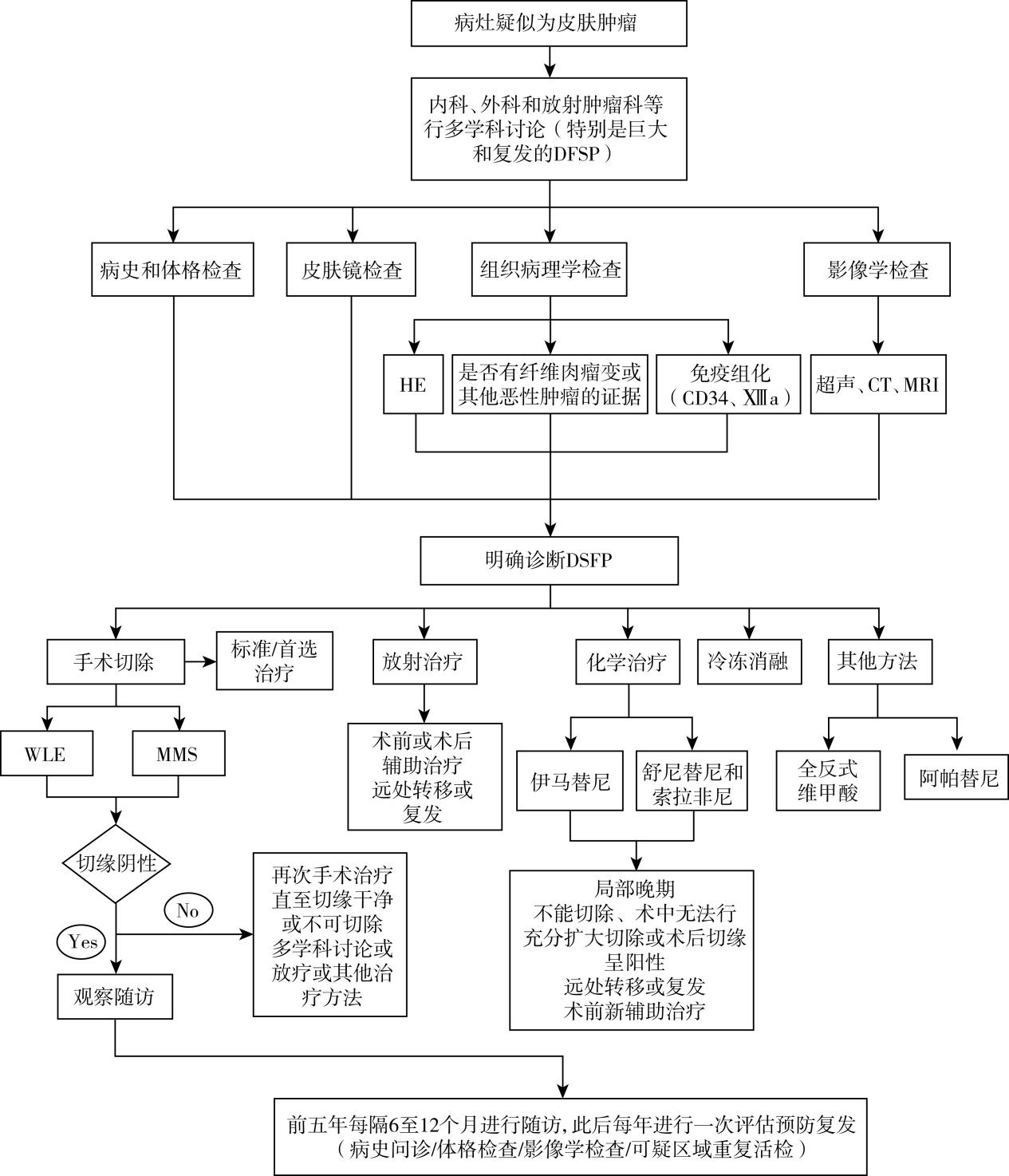
图22-1 DFSP诊疗流程
参考文献
[1] MULLEN JT. Dermatofibrosarcoma protuberans: wide local excision versus mohs micrographic surgery. Surg Oncol Clin N Am,2016,25(4):827-39.
[2] RAMIREZ-FORT MK, MEIER-SCHIESSER B, NIAZ MJ, et al. Dermatofibrosarcoma protuberans: the current state of multidisciplinary management. Skinmed,2020,18(5):288-293.
[3]陈友鑫,蔡震.隆突性皮肤纤维肉瘤发病机制及治疗进展.中华整形外科杂志,2022, 38(10):1193-1198.
[4] ALLEN A, AHN C, SANGÜEZA OP. Dermatofibrosarcoma protuberans. Dermatol Clin,2019,37(4):483-488.
[5] VITIELLO GA, LEE AY, BERMAN RS. Dermatofibrosarcoma protuberans: what is this?. Surg Clin North Am,2022,102(4):657-665.
[6] HAO X, BILLINGS SD, WU F, et al. Dermatofibrosarcoma protuberans: update on the diagnosis and treatment. J Clin Med,2020,9(6):1752.
[7] BADHEY AK, TIKHTMAN R, TANG AL. Management of dermatofibrosarcoma protuberans. Curr Opin Otolaryngol Head Neck Surg,2021,29(4):278-282.
[8] MUJTABA B, WANG F, TAHER A, et al. Dermatofibrosarcoma protuberans: pathological and imaging review. Curr Probl Diagn Radiol,2021,50(2):236-240.
[9] RUST DJ, KWINTA BD, GESKIN LJ, et al. Surgical management of dermatofibrosarcoma protuberans. J Surg Oncol,2023,128(1):87-96.
[10] HAO X, BILLINGS SD, WU F, et al. Dermatofibrosarcoma protuberans: update on the diagnosis and treatment. J Clin Med,2020,9(6):1752.


