136、冷凝集素病
罕见病诊疗指南(2025年版)
概述 冷凝集素病(cold agglutinin disease, CAD)是一种罕见的自身免疫性溶血性贫血,是冷抗体型自身免疫性溶血性贫血(cold autoimmune hemolytic anemia,cAIHA)中的重要类型,临床表现为冷凝集素(cold agglutininn,CA)介导的溶血性贫血及周围循环症状,部分患者会出现手足发绀,甚至血栓。原发性冷凝集素病(CAD)需要与继发性冷凝集素综合征(cold agglutinin syndrome,CAS)相鉴别。
病因和流行病学
冷凝集素(cold agglutinin,CA)是由B细胞产生的自身抗体,低温时凝集红细胞(red blood cell,RBC)启动补体介导的溶血。虽然CAD与CAS中都有CA,但两者的CA具有不同特征。首先,产生CA的细胞在CAD和继发于淋巴瘤的CAS中是单克隆的,在继发于感染的CAS中是多克隆的。此外,90%以上CAD患者的CA是对RBC表面I/i血型抗原特异的单克隆IgMκ,偶有对Pr抗原特异的;而CAS的CA是对I/i特异的IgG或IgM,轻链表型可以是λ或κ。
在CAD中,CA IgM重链85%以上是由14号染色体q臂上的IGHV4-34基因编码,该基因是CA活性的基础。IGHV4-34 FR1对识别I/i抗原至关重要。研究发现,许多患者的IGHV4-34 FR3发生了KLS序列突变,该突变增强了与I抗原结合的能力,而其突变数量与较低的血红蛋白水平相关。80%CAD患者的κ轻链是由IGKV3-20或IGKV3-15基因编码,这些基因也和I/i抗原的识别结合有关。
经典补体途径介导的血管外溶血被认为是CAD稳定期主要溶血机制。寒冷时CAD患者的CA结合RBC形成CA-RBC复合物,与C1q结合启动补体经典途径,顺序活化C1r、C1s、C4、C2生成C4b2a(C3转化酶),裂解C3为C3a和C3b。补体C3b致敏的RBC通过肝网状内皮系统时被巨噬细胞吞噬发生血管外溶血,大量补体消耗限制了溶血速率。而C3b结合C4b2a形成C4b2a3b(C5转化酶)裂解C5,导致膜攻击复合物(MAC)的形成,故15%的患者也可观察到血管内溶血。在高热、感染或重大手术等急性期,大量补体蛋白产生和末端途径激活,主要表现为血管内溶血。
冷凝集素病年发病率约为1/100万,占所有自身免疫性溶血性贫血(autoimmune haemolytic anaemias,AIHA)的13%~15%,是一种具有独特病理和遗传特征的淋巴增殖性疾病(lymphoproliferative disease,LPD),疾病状态常表现为慢性持续性。
临床表现
冷凝集素病临床表现呈多样性,发病速度、溶血程度和病程的变异性都很大。表现为慢性溶血性贫血和/或寒冷诱发的循环症状。绝大多数冷凝集素病患者有慢性溶血性贫血,伴或不伴有黄疸;可以出现间断、急性溶血伴寒冷诱发的血红蛋白尿。循环症状遇冷加重,常表现为末梢肢体发绀,甚至发生冻疮、坏疽,可有雷诺现象,遇暖好转。手足发绀及其他影响手指、脚趾、鼻及双耳的寒冷介导的血管闭塞现象与RBC沉积于皮下微血管有关。皮肤溃疡和坏死较为少见。肺炎支原体感染引发的CAS溶血起病急,特征性发生于肺炎恢复期,此时体内冷凝集素滴度正好达到峰值。溶血具有自限性,可持续1~3周。其他体征变化各异,脾脏肿大可见于原发性冷凝集素病。
辅助检查
1.特异性检查
(1)RBC自身抗体检查:①直接抗人球蛋白试验(direct antiglobulin test, DAT)检测被覆于红细胞膜的自身抗体,冷抗体型自身抗体与RBC最佳结合温度为0~5℃,多数患者IgG、IgA型抗体阴性,补体C3单独阳性。②间接抗人球蛋白试验(indirect antiglobulin test, IAT)检测血清中的游离抗红细胞膜抗体,多数患者呈阴性。③CA试验检测血清中CA,CA与RBC最佳结合温度为0~5℃,几乎所有患者阳性,效价滴度≥1∶64为阳性。
(2)病因学检查:无基础疾病者诊断为CAD,骨髓中常有单克隆κ链阳性的克隆性B淋巴细胞;有基础疾病则为CAS,常有确定的淋巴增殖性疾病、风湿结缔组织病或感染性疾病。
2.常规检测项目
(1)血常规及分类、血涂片、网织红细胞计数、肝肾功能(含胆红素及分类)、乳酸脱氢酶。
(2)抗核抗体、抗dsDNA抗体、类风湿因子、抗磷脂抗体、血清蛋白电泳、免疫固定电泳和IgG、IgA和IgM定量。有条件单位可检测B、T细胞亚群及相关细胞因子。
(3)HBV、HCV、HIV、EB病毒(EBV)、巨细胞病毒(CMV)、细小病毒B19和肺炎支原体。
(4)全身浅表淋巴结超声,胸部、腹部、盆腔CT。
(5)骨髓细胞形态学、骨髓病理、淋巴细胞流式免疫表型。
诊断
CAD诊断标准:①血红蛋白(HGB)水平达贫血标准;②血结合珠蛋白降低(<250 mg/L)、血总胆红素升高(≥ 17.1µmol/L,以非结合胆红素升高为主)、血乳酸脱氢酶升高且网织红细胞百分比> 4%或绝对值> 120×109/L;③检测到RBC自身抗体:自身抗体为C3d型(IgG型阴性或者弱阳性),并且冷凝激素(CA)效价≥1∶64;④排除其他基础疾病导致的CAS。
鉴别诊断
常见的需要与CAD鉴别的疾病包括:
1.CAS 多项研究都强烈表明CAD是与LPL/华氏巨球蛋白血症不同的实体。由于CAD是一种惰性疾病,不会发展为全身性淋巴组织增殖性疾病,故将其称为“原发性CA相关性LPD”,与继发于淋巴瘤的CAS相区别。CAD:自身抗体为C3d型(IgG型阴性或者弱阳性),并且冷凝激素(CA)≥1∶64(外周血或骨髓可以存在克隆性B淋巴细胞增殖,但没有恶性肿瘤的相关临床症状,影像学没有恶性肿瘤的证据)。CAS:自身抗体为C3d型(IgG型阴性或者弱阳性),并且CA≥1∶64。较少见,常继发于肺炎支原体、流感病毒感染及恶性肿瘤、实体瘤、自身免疫性疾病等,临床表现取决于原发病,可为一过性或持续性溶血。CAS引起的溶血常在原发病控制后明显改善,这一点明显不同于CAD。
2.阵发性睡眠性血红蛋白尿 也会出现贫血以及血红蛋白尿,与阵发性冷性血红蛋白尿相似,但前者与寒凉刺激无关,冷溶血实验为阴性,酸溶血试验、糖水试验呈阳性,流式细胞术可检测到CD55、CD59缺陷细胞,可与后者鉴别。
3.血栓性血小板减少性紫癜 属于微血管病性溶血,其抗人球蛋白试验阴性,且血涂片除有周缘不规则的小球形细胞外,尚有大量红细胞碎片存在,可与CAD鉴别。
4.遗传性球形红细胞增多症 是RBC膜有先天缺陷的一种溶血性贫血,主要表现为贫血、黄疸、脾肿大,与CAD相似,但一般自幼起病且有家族史,抗人球蛋白试验阴性,红细胞渗透脆性试验阳性。
5.其他可引起雷诺现象的疾病 与CAD有相似之处,均会有四肢末端发绀等现象,但发绀与寒冷无关,且冷凝集试验为阴性。
治疗
CAD治疗包括非药物治疗和药物治疗,轻症患者通过保暖、输液加温、防治感染等非药物治疗即可改善,非药物治疗效果不佳、症状性贫血、输血依赖或出现严重影响生活的循环系统症状时可选择药物治疗。药物治疗包括一般治疗、针对B细胞的治疗以及补体抑制剂的治疗。一般治疗包括糖皮质激素、细胞毒药物、脾切除术等,疗效较差。针对产生CA的B细胞的治疗优点是对溶血及循环症状均有效,缺点是起效较慢,对急性溶血控制不佳。补体抑制剂起效快,CAD及CAS均有效,可用于急性溶血,但需长期维持治疗,且无法改善RBC凝集所致的周围循环症状。
1.一线治疗 利妥昔单抗(rituximab,RTX)是一种人鼠嵌合型单克隆CD20抗体,为CAD一线治疗方案。
(1)利妥昔单抗单药:利妥昔单抗375 mg/m2,每周1次,连续4次。有效率50%左右,但CR率较低(3%)。疗效持续时间少于1年。复发后,再次应用多有效。不良反应多轻微。
(2)利妥昔单抗联合苯达莫司汀:利妥昔单抗375mg/m2,第1天;苯达莫司汀70~90 mg/(m2·d),第1、2天。28 d为1个疗程,共4个疗程。有效率为71%,其中CR率为40%。中位起效时间1.9个月。疗效持久,中位随访32个月,复发率仅9%。主要不良反应是粒细胞减少和发热等。
(3)利妥昔单抗联合氟达拉滨:利妥昔单抗375 mg/m2,第1天;氟达拉滨25 mg/(m2·d),第1~5天。四周为1个疗程,共4个疗程。有效率为76%,其中CR率为21%,PR率为55%。中位起效时间4个月,中位疗效持续时间66个月。主要不良反应是骨髓抑制和感染等。
2.二线治疗 如果一线治疗方案是利妥昔单抗单药,无效和复发后,可以选择利妥昔单抗联合苯达莫司汀/氟达拉滨治疗。如果1年后复发,也可选择利妥昔单抗单药治疗。
如果一线治疗方案是利妥昔单抗联合苯达莫司汀/氟达拉滨,无效和短期复发(1年内),可以选择临床试验或者BTK抑制剂如伊布替尼或以下方案。如果2年后复发,也可选择再次应用利妥昔单抗联合苯达莫司汀/氟达拉滨治疗。
(1)伊布替尼:13例CAD/CAS患者应用伊布替尼(420 mg/d)治疗,有效率为100%,其中12例CR,1例PR。HGB中位升高56 g/L。全部患者3个月内脱离输血。多数患者1个月内起效,贫血和溶血减轻,雷诺现象缓解。不良反应为轻度皮肤瘀斑、腹泻和皮疹等。
(2)硼替佐米:硼替佐米常用剂量为1.3 mg/m2,每周1次,连续4次为一疗程。有效率为31%。主要不良反应包括神经毒性、骨髓抑制、腹泻、便秘等。
(3)达雷妥尤单抗是针对浆细胞和淋巴浆细胞表面跨膜糖蛋白CD38的单克隆抗体,已证明对多发性骨髓瘤有效。2020年和2021年各报道了一例达雷妥尤单抗在复发难治的CAD患者中取得良好疗效的病例,在经过8个周期和19个周期达雷妥尤单抗后患者HGB均增长> 30 g/L,溶血及循环症状消失,脱离输血,其中一例患者观察到CA滴度的下降和骨髓改善,这为达雷妥尤单抗用于CAD患者提供了依据。
3.补体抑制剂:补体C1抑制剂苏替利单抗(sutimlimab)、C3抑制剂pegcetacoplan和C5抑制剂依库珠单抗(eculizumab)能迅速控制部分CAD/CAS患者溶血发作,改善贫血。
4.其他药物和治疗方法 静脉免疫球蛋白对部分CAD患者有效。血浆置换对IgM型冷抗体效果较好(37℃时80%IgM型抗体呈游离状态),但对其他吸附在RBC上温抗体效果不佳,且置换带入大量补体。
并发症监测
1.红细胞成分输血 (1)应尽量避免或减少输血。(2)输血时机应根据贫血程度、有无明显症状、发生快慢而定。对于急性溶血性贫血患者,出现严重症状时能排除同种抗体者须立刻输注红细胞。对于慢性贫血患者,HGB在70 g/L以上不必输血;HGB在50~70 g/L时如无不能耐受的症状可不输血;HGB在50 g/L以下时建议输血。(3)抢救时不强调应用洗涤红细胞。(4)CAD患者红细胞输注时应注意保温。
2.清除溶血产物和保护重要脏器功能 碱化利尿、利胆去黄,并注意电解质平衡。
3.感染的预防和治疗 CAD患者自身免疫紊乱、糖皮质激素和免疫抑制剂治疗等都会明显增加感染(尤其是致命重度感染)的风险,应注意感染的预防。有条件者可以接种相关疫苗。一旦感染,应积极寻找感染灶和病原体,有针对性的抗感染治疗。
4.血栓的预防 11%~20%AIHA患者发生血栓,血栓事件发生率明显高于年龄性别匹配的正常人群,包括肺栓塞、深静脉血栓、脾栓塞、脑卒中和心肌梗死等。血栓的危险因素包括急性溶血发作、卧床、发热、高龄、既往血栓病史、易栓症、创伤或外科手术、呼吸衰竭、心力衰竭、感染等。合并高危因素患者常规应用抗凝治疗预防血栓的发生,常用药物包括低分子肝素或口服抗凝药。
诊疗流程(图15-1)
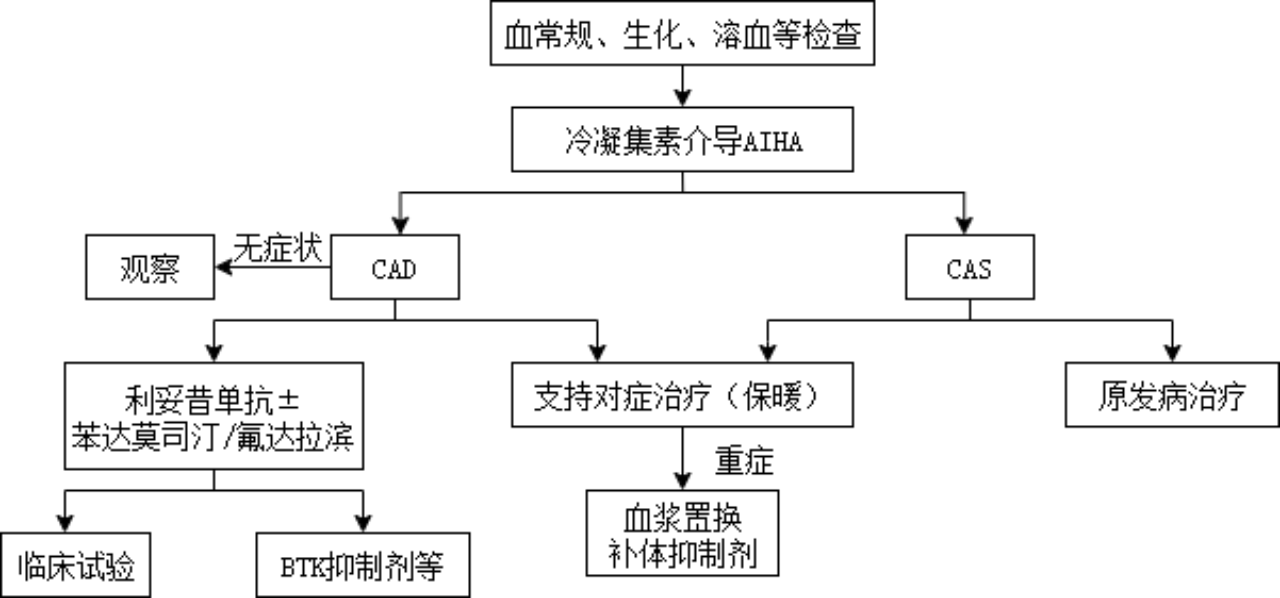
图15-1 冷凝集素病诊治流程
参考文献
[1] 中华医学会血液学分会红细胞疾病(贫血)学组.中国成人自身免疫性溶血性贫血诊疗指南(2023年版).中华血液学杂志,2023,44(1):12-18.
[2] 刘京倩, 张凤奎.冷凝集素疾病的诊疗进展.中华血液学杂志,2022,43(6):524-528.
[3] BERENTSEN S, BARCELLINI W. Autoimmune hemolytic anemias. N Engl J Med, 2021,385(15):1407-1419.
[4] BERENTSEN S. How I treat cold agglutinin disease. Blood,2021,137(10):1295-1303.
[5] RÖTH A, BARCELLINI W, D'SA S, et al. Sustained inhibition of complement C1s with sutimlimab over 2 years in patients with cold agglutinin disease. Am J Hematol,2023,98(8):1246-1253.
[6] ROSSI G, GRAMEGNA D, PAOLONI F, et al. Short course of bortezomib in anemic patients with relapsed cold agglutinin disease: a phase 2 prospective GIMEMA study. Blood,2018,132(5):547-550.


