综述 | 原发性纤毛运动障碍患者外显子组测序阴性后的遗传诊断思路
中国罕见病联盟
原发性纤毛运动障碍(PCD)是一种罕见的单基因遗传病,主要与动纤毛结构和功能障碍有关,多呈常染色体隐性遗传。该疾病会累及多个器官,并且患者的临床表型与遗传异质性为其诊断带来了极大的困难。尽管临床上外显子组测序的使用大大提高了PCD的诊断率,但仍有约30%以上的患者未能得到有效的诊断。本文对PCD的发病机制、诊断方法及外显子组测序阴性后的诊断思路和新兴遗传检测技术进行综述和探讨,以期帮助临床医师进一步选择更多的新兴遗传检测方法,从而提高PCD的阳性诊断率,并提高临床医师对其遗传致病机制的深刻理解,为将来实践基因治疗奠定基础。
原发性纤毛运动障碍(primary ciliary dyskinesia,PCD)是一种由运动纤毛功能异常引起的罕见遗传病,具有较强的临床和遗传异质性,多为常染色体隐性遗传,也有X连锁隐性遗传和常染色体显性遗传(新发突变)的报道[1-2]。该疾病为一种累及多器官的动纤毛病,会导致慢性呼吸道疾病、生育问题及脑积水[3],还可能导致内脏转位或先天性心脏缺陷等[4]。目前,由于地域、人种及数据来源的不同,PCD的发病率差异很大,已报道的发病率为1/40 000~1/10 000[5-6]。值得注意的是,国内对PCD患者的报道较少,PCD患者临床表现的异质性可能导致漏诊或误诊[7]。在临床上,外显子组测序(exome sequencing,ES)的使用显著提高了疾病的诊断率,诊断率从25%到40%不等[8-9]。据报道,PCD的阳性诊断率较高,可达70%左右[10-11],但超过30%的临床拟诊PCD患者在使用ES后仍未被诊断。本文将对PCD的发病机制、诊断方法及ES阴性后的诊断思路和新兴遗传检测技术进行综述和探讨,以期帮助临床医师进一步选择更多新兴遗传检测方法,从而提高PCD的阳性诊断率,并提高临床医师对其遗传致病机制的深刻理解。
1发病机制
纤毛和鞭毛是在生物进化过程中高度保守的结构。纤毛主要由基体、轴丝、纤毛膜和纤毛基质组成,突起于细胞表面。纤毛分为动纤毛和不动纤毛两类。
动纤毛是一种复杂且特殊的毛发状细胞器,能有节奏地摆动,在气道、鼻窦和咽鼓管中运输液体和黏液并可以沿上皮表面捕获细菌[12]。每个气道上皮细胞约有200个动纤毛聚集在其表面[13],正常的动纤毛和黏液对气道有效清除起着重要作用,任何干扰动纤毛精确、协调摆动的改变都可能导致动纤毛病[14]。除呼吸道外,在脑室和输卵管的一些上皮细胞上也有丰富的动纤毛[15-16]。
动纤毛主要分为两种类型,分别为具有完整“9+2”微管结构的动纤毛和具有“9+0”微管结构的胚节动纤毛[17]。动纤毛的核心部分是由一个中心粒衍生出的微管核心,称为轴丝。在电镜下,轴丝的横切面呈现“9+2”的结构,即由9对外周微管环绕着1对中央微管组成。外周微管与中央微管之间通过辐射臂相连并固定。外周微管之间则通过微管连接蛋白连接,外周微管的内、外分别连接内动力臂和外动力臂[18](图1)。
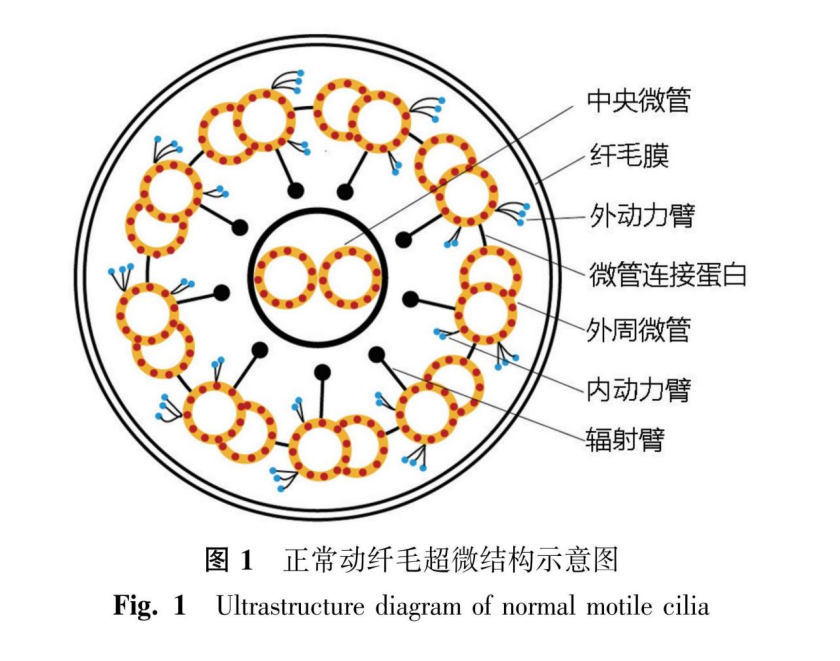
中央微管在动纤毛摆动过程中发挥了关键作用,其不仅可以保持动纤毛结构的完整性,还可以传递动力和排列相邻的纤毛,以确保动纤毛能沿气道做同一方向的摆动[14]。外动力臂中的轴索动力蛋白是一种多头运动蛋白,其可以通过ATP酶活性产生动力,进而转化为两个相邻小管的滑动运动。内动力臂则通过连接蛋白-动力蛋白调节复合物调节微管滑动和纤毛运动,该复合物由多个蛋白质组成,协调多个动力蛋白的活性从而控制纤毛摆动[19]。
PCD是一种具有遗传异质性的疾病,目前已报道过50多个 PCD 致病基因[20-21]。在这些基因中,绝大部分编码的是动纤毛或精子鞭毛轴丝内多种蛋白质、纤毛膜和基体中的蛋白质,或者是纤毛正确组装所需的蛋白质[10]。此外,还有少数致病基因与动纤毛的生成和分化成熟过程有关[22]。
2国内外诊断标准
2.1临床诊断
由于PCD为罕见病,临床医师对其认识不足,并且其诊断需要专门检测,因此临床诊断PCD较为困难。2016年,美国胸科学会(American Thoracic Society,ATS)将以下4个临床特征定义为PCD的预测指标,包括侧性缺陷、不明原因的新生儿呼吸窘迫、早发性和全年鼻塞及湿咳[23]。这些特征是PCD诊断的重要临床线索。
欧洲呼吸学会(European Respiratory Society,ERS)和ATS近年来分别发布了关于PCD的诊断指南。这两份指南均提出,目前尚无任何一种方法可以独立地诊断PCD,大多数检测方法的灵敏度和特异性均较低,且需要专业设备和知识。因此,该指南建议进行一系列综合测试,包括鼻NO浓度、高速视频显微镜分析(high-speed video microscopy analysis,HSVMA)、免疫荧光、透射电子显微镜(transmission electron microscope,TEM)和基因检测[24]。对于临床PCD的诊断,需要满足以下要求:①患者的临床表型需要与疾病相符;②至少通过以下两种方法进行确认:HSVMA发现明确纤毛运动异常、TEM发现明确纤毛结构异常、免疫荧光显微镜发现明确纤毛相关蛋白表达异常、鼻NO浓度异常低,或基因检测找到明确的双等位基因致病变异[21]。
中国专家推荐采用以下临床诊断标准[18]:①符合PCD临床特征中至少2项(足月儿发生不明原因的新生儿呼吸窘迫综合征,半岁之前开始常年持续咳嗽,半岁之前开始常年持续鼻塞,内脏反位);②TEM检查发现典型的纤毛超微结构缺陷(外动力臂缺失、外动力臂和内动力臂联合缺失、内动力臂缺失合并微管排列紊乱,以及中央微管缺失);③基因检测发现PCD已知致病基因的双等位基因致病变异。当患者表型符合①、②或①、③即可确诊为PCD。
2.2基因诊断
对于PCD的基因诊断,由于参与动纤毛结构和功能的蛋白质超过200种[25],而目前仅发现50多个PCD致病基因[17],还有很多可能的PCD新致病基因有待发现,因此基因检测本身不能作为PCD诊断的金标准。然而,随着二代测序技术的进步、测序成本的降低,以及生物信息学的发展,PCD的基因诊断也日益得到关注。这些进步为提高PCD的诊断率和更深入地理解PCD的发病机制提供更多可能。
二代测序中ES可以在单个碱基对层面上检测与遗传病因相关的基因变异。人类基因组约有180 000个外显子,仅占整个基因组1%,但据估计85%的致病变异都源自蛋白编码区和剪接位点[26]。而ES就是利用序列捕获或靶向技术,将全基因组外显子区域的DNA富集后再进行高通量测序,从而实现对外显子组的分析。由于ES对外显子及其侧翼区域变异位点的检测具有很高的灵敏度和特异性,因此在疾病基因的识别和分子诊断方面,ES展现出极大的优势[26-27]。
据报道,临床拟诊PCD患者经ES后仍有超过30%的个体未找到致病变异[10-11]。因此,目前迫切需要总结ES阴性后的诊断思路,为临床医师选择较好的后续检测方法提供借鉴。
3外显子组测序阴性后的诊断思路
在ES检测后,PCD患者仍未被诊断可能包括以下两种情况:一是未找到候选致病基因与变异,二是找到的候选基因与变异被评估为临床意义未明。对于未找到候选致病基因与变异又可细分为两种情况:①完全未找到候选致病基因与变异;②只找到隐性遗传病中一个致病变异位点。针对这些问题,下文将讨论几种技术,针对不同情况解决ES检测后未诊断PCD病例的基因确诊问题(表1)。

3.1ES数据重分析
在患者ES数据重分析未诊断一段时间后,由于新致病基因的发现、临床意义未明变异的重新解读及生物信息学的进步,对现有的ES数据进行重新分析可能会发现新的致病变异。通过ES重分析得出的诊断结果主要可以分为两大类:一类是前次分析中遗漏的变异,通常包括插入缺失、编码区两侧的非编码变异或拷贝数变异(copy-number variants,CNVs);另一类是候选的临床意义未明变异,这需要实验室和临床医师对这些变异进行重新解读。实际上,所有通过对ES数据重分析得出的诊断,都需要用新的证据来支持这些变异的致病性。近期一项调查显示,在27项相关研究中,通过ES数据重分析,疾病诊断率提高了约15%,并建议自原始分析完成18个月后,对数据重新分析以优化诊断结果[28]。
ES重分析是由美国医学遗传学与基因组学学会正式推荐的检测技术,可以根据临床医师要求,实验室定期对临床拟诊PCD患者进行ES重分析[29],以最大程度地发挥ES检测技术在临床诊断中的功效。
3.2基因组测序
与ES相比,基因组测序(genome sequencing,GS)是对整个基因组进行测序,提供可以识别几乎所有临床相关变异的平台,能够分析编码区和非编码区的变异。这种技术能检测到ES无法覆盖区域的变异,并能检测到染色体结构变异(structural variants,SVs),包括CNVs、染色体倒位、易位和短串联重复等。此外,GS的显著优势是其能够在一次测序中检测到多种类型的变异,从而提高检测效率。
GS理论上可以发现被ES遗漏的非编码区变异和SVs,同时也为识别新的致病基因提供可能。在英国一项10万基因组计划项目中,21例未被ES诊断的PCD先证者接受GS专业分析,其中有16例得到有效的评估[确诊(n=9)、极为可能(n=4)或可能(n=3)][30]。值得注意的是,研究小组在该队列中发现了两个新的PCD候选致病基因(IFT140和PLK4)的变异,推动了PCD致病机制研究的发展。
然而,与ES和基因panel相比,GS的数据生成成本较高、分析负担较重且平均覆盖率较低。此外,由于成本的限制,目前GS的临床应用不及ES普遍。以上因素都需要临床医师在选择使用GS前进行综合考虑。
3.3RNA测序
尽管GS可以捕获各种类型的变异,但仍不能评估一些内含子和基因间区等非编码区变异对蛋白质功能的影响,这可能导致一些潜在的致病变异被遗漏。一部分ES阴性可能归因于一些远离剪接供体-受体位点的非经典剪接变异[31]。RNA测序(RNA sequencing,RNA-seq)不依赖于对疾病潜在变异位点的认识,可根据基因的表达或剪接来识别导致疾病的基因[32]。
在日本进行的一项研究中,研究者收集36例PCD患者的样本,利用呼吸道黏膜特异性RNA-seq,将测序读数映射到人类基因组上,并使用FRASER工具[33]对所有数据进行分析。FRASER 是一种控制潜在混杂因素后从统计学角度提取异常剪接事件的工具。最终在9例患者中发现异常的剪接事件,包括内含子异常保留、外显子跳跃及大片段缺失,为PCD患者的诊断提供直接的证据[34]。
从上述研究中可以得知,转录组图谱在很大程度上取决于所采集的组织样本和患者的临床状态,并非所有的基因都在容易获得的组织中表达。若在PCD患者中,某些纤毛相关基因在外周血中不表达或表达量极低,则要考虑通过支气管镜取患者呼吸道黏膜或支气管组织。尽管存在这些局限性,RNA-seq已成功地用于为临床意义未明变异的重新解读提供证据和识别遗漏的致病变异。根据所研究的表型和组织测序的不同,RNA-seq报告的诊断率为7.5%~34%[35-36]。
3.4长读长基因组测序
与GS相比,长读长基因组测序(long-read genome sequencing,lrGS)能更好地映射到基因组的重复区域,从而可以较准确识别致病SVs[37-38]。
有研究表明,在无法用GS分析的基因组区域中,lrGS技术有助于识别基因与表型的关联[39-40]。但是,与GS数据一样,lrGS用于解释非编码单核苷酸变异、Indels和SVs的工具依然较少。在临床实践中,需要根据分析工具不断变化的管线和有限的参考数据集(特别是不同人群)来判断lrGS是否适用于筛选特定的病例[41]。
理论上来说,可能存在复杂SVs导致的PCD患者。截至2024年4月,PubMed、Google Scholar、Web of Science未检索到利用lrGS协助确诊PCD患者的文献报道。
3.5光学基因组图谱
光学基因组图谱(optical genome mapping, OGM)是一种通过成像荧光标记的技术,用于比较样本与参考基因组之间的荧光标记模式,以识别SVs。OGM能够检测用其他方法难以检测的SVs,如<25 kb的CNVs或平衡倒位与易位[42]。
虽然OGM在检测SVs、大CNVs和复杂的基因组重排方面表现出色,但其分辨率受到基因组荧光标签之间的间距和成像光电池分辨率的限制。对于临床应用,OGM检测变异只是第一步,进一步确定SVs的临床相关性是一个主要挑战。
理论上来说,可能存在复杂基因组重排导致的PCD患者。截至2024年4月,PubMed、Google Scholar、Web of Science未检索到利用OGM协助确诊这类PCD患者的文献报道。
3.6多组学方法
整合生化和蛋白质组数据,使用多种数据类型组合的多组学方法,如基因组、转录组、表观遗传学、蛋白质组、代谢组或生化数据,称为多组学方法[43-44]。尽管将大量数据与这些方法中的任何一种相结合都有一定的挑战性,但总体思路是在可用于变异识别和优先排序的数据中寻找重叠线索。相互补充的不同组学技术整合可以为在进行广泛的临床检测后仍未确诊的患者提供关键线索。
3.7补充功能实验
若发现的候选基因与变异被评估为临床意义未明,则可酌情进行相关功能实验,以补充致病证据。例如,构建变异的真核表达载体,以检测变异后蛋白的表达量。若变异经软件预测可能会导致异常剪接,则可进行Mini gene实验,即在体外构建含有突变位点的部分外显子及内含子的载体,然后将其转染到工具细胞中,运用RT-qPCR和测序技术,分析基因变异对pre-mRNA序列的影响[45]。
4结语
PCD是一种具有遗传异质性的罕见疾病,在中国目前诊断率较低可能是由于多种因素,包括技术限制、临床医师对变异致病性的不完全理解、缺失基因型-表型之间的关联、复杂的基因-环境相互作用,以及临床实验室之间的报告差异等。
尽管ES在临床使用大大提高了PCD的诊断率,但超过30%的PCD患者在进行ES检测后仍未找到致病变异。针对这些未能找到致病变异的临床拟诊患者,本文提出了一系列的建议(图2)。
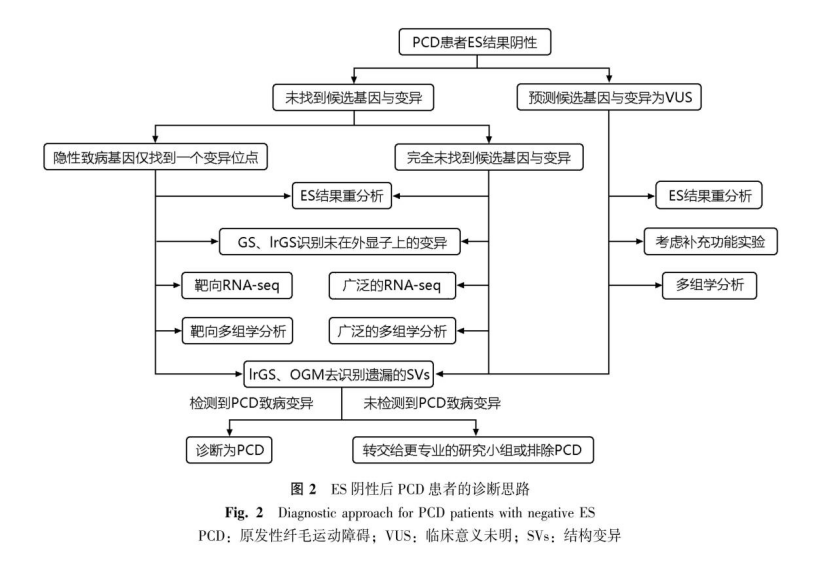
首先,建议对于ES检测后未能获得诊断的拟诊PCD患者,至少进行一次ES结果重分析,特别是在初次检测或最后一次分析已超过一年的情况下。其次,对于在ES检测后未找到候选基因与变异的临床拟诊PCD患者,可分为在隐性PCD致病基因中发现单个候选基因与变异和完全未找到PCD候选基因与变异两种情况。
当在已知隐性PCD基因中发现了单个变异,应使用更多新兴的遗传检测技术进一步评估。相关的遗传检测技术包括GS、靶向RNA-seq、靶向多组学分析和lrGS、OGM识别其他方法遗漏的SVs等。对于未明确的候选基因或变异进行探索的个体,应采取更广泛的方法,如GS或广泛的RNA-seq和多组学分析。然而,目前只有少数的临床实验室能提供非靶向RNA-seq,且无法对其结果进行系统评估。通过GS或lrGS扩大基因筛选范围可能会提高二次发现变异或新致病基因的能力。
最后,当在已知PCD致病基因中发现的变异被评估为临床意义未明时,可以根据具体情况设计功能实验进行补充验证或进行多组学分析来明确变异的致病性。若经上述检测仍未找到可以评估为PCD的致病变异,则建议转交给更专业的研究小组或排除PCD的可能性。
总之,临床医师需要根据患者的表型或临床拟诊来确定在ES阴性后是否需要选择更多新兴遗传检测技术来鉴定可能的致病变异。根据文献报道与临床诊断经验来说,ES与GS合并RNA-seq是目前最适合PCD拟诊患者的诊断策略。此外,SVs是一种可能的PCD致病变异类型,因此在其他方法都阴性时,lrGS或OGM也是可供选择的检测技术。这些新兴的遗传检测技术在提高PCD阳性诊断率的同时,可以更好地理解PCD的遗传致病机制,为PCD将来的精准靶向基因治疗提供分子基础。
作者贡献:李奕璇负责文献检索、综述初稿撰写;何苗、郑海霞负责论文整合与修订;刘雅萍负责审校修改。
利益冲突:所有作者均声明不存在利益冲突。
参考文献
[1]Wallmeier J,Frank D,Shoemark A,et al. De novo mutations in FOXJ1 result in a motile ciliopathy with hydroce-phalus and randomization of left/right body asymmetry[J]. Am J Hum Genet,2019,105(5):1030-1039.
[2] Knowles MR,Zariwala M,Leigh M. Primary ciliary dyskinesia[J]. Clin Chest Med,2016,37(3):449-461.
[3]Wallmeier J,Nielsen KG,Kuehni CE,et al. Motile ciliopathies[J]. Nat Rev Dis Primers,2020,6(1):77.
[4]Shapiro AJ,Davis SD,Ferkol T,et al. Laterality defects other than situs inversus totalis in primary ciliary dyskinesia:insights into situs ambiguus and heterotaxy[J]. Chest,2014,146(5):1176-1186.
[5]Kuehni CE,Frischer T,Strippoli MP,et al. Factors influ-encing age at diagnosis of primary ciliary dyskinesia in European children[J]. Eur Respir J,2010,36(6):1248-1258.
[6]O'Callaghan C,Chetcuti P,Moya E. High prevalence of primary ciliary dyskinesia in a British Asian population[J]. Arch Dis Child,2010,95(1):51-52.
[7]Guan Y,Yang H,Yao X,et al. Clinical and genetic spectrum of children with primary ciliary dyskinesia in China[J]. Chest,2021,159(5):1768-1781.
[8]Yang Y,Muzny DM,Xia F, et al. Molecular findings among patients referred for clinical whole-exome sequencing[J]. JAMA,2014,312(18):1870-1879.
[9]Retterer K,Juusola J,Cho MT, et al. Clinical application of whole-exome sequencing across clinical indications[J]. Genet Med,2016,18(7):696-704.
[10]Pioch CO,Connell DW,Shoemark A. Primary ciliary dyskinesia and bronchiectasis:new data and future challenges[J]. Arch Bronconeumol,2023,59(3):134-136.
[11]Lucas JS,Davis SD,Omran H,et al. Primary ciliary dyskinesia in the genomics age[J]. Lancet Respir Med,2020,8(2):202-216.
[12]Leigh MW,Pittman JE,Carson JL, et al. Clinical and genetic aspects of primary ciliary dyskinesia/Kartagener syndrome[J]. Genet Med,2009,11(7):473-487.
[13]Horani A,Ferkol TW. Understanding primary ciliary dyskinesia and other ciliopathies[J]. J Pediatr,2021,230:15-22.e1.
[14]Horani A,Ferkol TW. Advances in the genetics of primary ciliary dyskinesia:clinical implications[J]. Chest,2018,154(3):645-652.
[15]Banizs B,Pike MM,Millican CL,et al.Dysfunctional cilia lead to altered ependyma and choroid plexus function,and result in the formation of hydrocephalus[J]. Development,2005,132(23):5329-5339.
[16]Raidt J,Werner C,Menchen T,et al. Ciliary function and motor protein composition of human fallopian tubes[J]. Hum Reprod,2015,30(12):2871-2880.
[17]Niziolek M,Bicka M,Osinka A,et al. PCD genes-from patients to model organisms and back to humans[J]. Int J Mol Sci,2022,23(3):1749.
[18]中国罕见病联盟呼吸病学分会,原发性纤毛运动障碍诊断与治疗中国共识专家组. 原发性纤毛运动障碍诊断与治疗中国专家共识[J]. 上海医学,2020,43(4):193-202.
[19]Heuser T,Raytchev M,Krell J, et al. The dynein regulatory complex is the nexin link and a major regulatory node in cilia and flagella[J]. J Cell Biol, 2009,187(6):921-933.
[20]Shapiro AJ,Zariwala MA,Ferkol T,et al. Diagnosis,monitoring,and treatment of primary ciliary dyskinesia:PCD foundation consensus recommendations based on state of the art review[J]. Pediatr Pulmonol,2016,51(2):115-132.
[21]Lucas JS,Burgess A,Mitchison HM,et al. Diagnosis and management of primary ciliary dyskinesia[J]. Arch Dis Child,2014,99(9):850-856.
[22]Legendre M,Zaragosi LE,Mitchison HM. Motile cilia and airway disease[J]. Semin Cell Dev Biol,2021,110:19-33.
[23]Leigh MW,Ferkol TW,Davis SD, et al. Clinical features and associated likelihood of primary ciliary dyskinesia in children and adolescents[J]. Ann Am Thorac Soc,2016,13(8):1305-1313.
[24]Lucas JS,Barbato A,Collins SA,et al. European Respiratory Society guidelines for the diagnosis of primary ciliary dyskinesia[J]. Eur Respir J,2017,49(1):1601090.
[25]Reiter JF,Leroux MR. Genes and molecular pathways underpinning ciliopathies[J]. Nat Rev Mol Cell Biol,2017,18(9):533-547.
[26]李萌萌, 郝娜, 吕嬿, 等. 全外显子组测序技术在胎儿遗传病诊断中的应用进展[J]. 实用妇产科杂志,2023,39(3):171-175.
[27]罗东凤,王少元. 全基因组外显子测序及其在遗传病研究中的应用[J]. 国际遗传学杂志,2012,35(3):173-177.
[28]Tan NB,Stapleton R,Stark Z, et al. Evaluating systematic reanalysis of clinical genomic data in rare disease from single center experience and literature review[J].Mol Genet Genomic Med,2020,8(11):e1508.
[29]Deignan JL,Chung WK,Kearney HM,et al. Points to consider in the reevaluation and reanalysis of genomic test results:a statement of the American College of Medical Genetics and Genomics (ACMG)[J]. Genet Med,2019,21(6):1267-1270.
[30]Wheway G,Thomas NS,Carroll M, et al. Whole genome sequencing in the diagnosis of primary ciliary dyskinesia[J].BMC Med Genomics,2021,14(1):234.
[31]Shapiro AJ,Stonebraker JR,Knowles MR,et al. A deep intronic,pathogenic variant in DNAH11 causes primary ciliary dyskinesia[J].Am J Respir Cell Mol Biol,2022,67(4):511-514.
[32]Ferraro NM,Strober BJ,Einson J, et al. Transcriptomic signatures across human tissues identify functional rare genetic variation[J]. Science,2020,369(6509):eaaz5900.
[33]Mertes C,Scheller IF,Yépez VA, et al. Detection of aberrant splicing events in RNA-seq data using FRASER[J].Nat Commun,2021,12(1):529.
[34]Hijikata M,Morimoto K,Takekoshi D, et al. Analysis of aberrant splicing events and gene expression outliers in primary ciliary dyskinesia[J]. Am J Respir Cell Mol Biol,2023,68(6):702-705.
[35]Lee H,Huang AY,Wang LK, et al. Diagnostic utility of transcriptome sequencing for rare Mendelian diseases[J]. Genet Med,2020,22(3):490-499.
[36]Frésard L,Smail C,Ferraro NM,et al. Identification of rare-disease genes using blood transcriptome sequencing and large control cohorts[J]. Nat Med,2019,25(6):911-919.
[37]Mahmoud M,Gobet N,Cruz-Dávalos DI,et al. Structural variant calling: the long and the short of it[J]. Genome Biol,2019,20(1):246.
[38]Sedlazeck FJ,Lee H,Darby CA,et al. Piercing the dark matter:bioinformatics of long-range sequencing and map-ping[J]. Nat Rev Genet,2018,19(6):329-346.
[39]Cohen ASA,Farrow EG,Abdelmoity AT, et al. Genomic answers for children:dynamic analyses of >1000 pediatric rare disease genomes[J]. Genet Med,2022,24(6):1336-1348.
[40]Wagner J,Olson ND,Harris L, et al. Curated variation benchmarks for challenging medically relevant autosomal genes[J].Nat Biotechnol,2022,40(5):672-680.
[41]Beyter D,Ingimundardottir H,Oddsson A,et al. Long-read sequencing of 3,622 Icelanders provides insight into the role of structural variants in human diseases and other traits[J].Nat Genet,2021,53(6):779-786.
[42]Chan S,Lam E,Saghbini M, et al. Structural variation detection and analysis using bionano optical mapping[J]. Methods Mol Biol,2018,1833:193-203.
[43]Stenton SL,Kremer LS,Kopajtich R, et al. The diagnosis of inborn errors of metabolism by an integrative "multi-omics" approach:a perspective encompassing genomics,transcri-pto-mics,and proteomics[J]. J Inherit Metab Dis,2020,43(1):25-35.
[44]Khan S,Ince-Dunn G,Suomalainen A,et al. Integrative omics approaches provide biological and clinical insights:examples from mitochondrial diseases[J]. J Clin Invest,2020,130(1):20-28.
[45]Steffensen AY,Dandanell M,Jnson L, et al. Functional characterization of BRCA1 gene variants by mini-gene splicing assay[J]. Eur J Hum Genet,2014,22(12):1362-1368.


